Образование - поверхностный комплекс
Cтраница 1
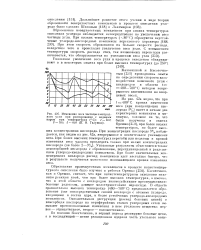 |
Изменение веса частицы электродного угля при реагировании с водяным паром при температурах ( С. 1 - 500. 2 - 550. 3 - 600 ( П. Н. Галушко. [1] |
Образование поверхностных комплексов при низких температурах окисления углерода наблюдается непосредственно по увеличению веса частицы угля. При этом скорость образования их больше скорости распада, вследствие чего и происходит увеличение веса угля. [2]
Это приводит к образованию отрицательно заряженного поверхностного комплекса и свободной дырки в объеме полупроводника. Поверхностное состояние электронного энергетического уровня будет зависеть от энергии связи в поверхностном комплексе, акцептирующем электрон. [3]
Хемосорбция, проявляющаяся в образовании поверхностного комплекса и последующем его р западе, может тормозить общую скорость реакции. [4]
Дауден [31], рассматривая хемосорбцию как процесс образования поверхностных комплексов и применяя расчеты по теории кристаллического поля, показал существенную связь каталитической активности окислов и сульфидов переходных металлов со степенью заполнения d - оболочки. [5]
Взаимодействие тиоэфира с твердым катализатором приводит к образованию поверхностного комплекса с переносом заряда от атома серы тиоэфира к атому металла катализатора ( см. гл. При определенной степени переноса заряда тиоэфир хемосорбируется без разрушения структуры, но активируется атом серы с локализацией на нем некоторого положительного заряда. Этот процесс может протекать на окислах металла в инертной атмосфере, но он должен существенно ускоряться в среде кислорода, так как убыль поверхностного кислорода будет восполняться из газовой фазы. [6]
По мнению Л. Я. Марковского [6, 113] добавки не толька облегчают образование поверхностных комплексов, но и снижают температуру их разрушения. Катионы добавок, внедряясь в межбазисное пространство, насыщают металлические валентности графита и уменьшают прочность связей в гексагональных сетках. [7]
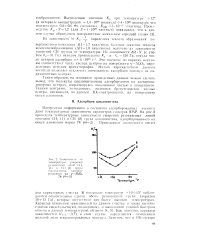 |
Зависимости от температуры yuuipeintii резонансных. ninnii Gib ( i п СП ( 2 групп цп клопе птепа, адсорбированного на Y-АЬОз 78 ( 0 2. [8] |
Из зависимости In Kv - - определена теплота образования поверхностного комплекса АН1 7 ккал / моль. Близкое значение теплоты комплексообразованпя ( АН 1 8 ккал / моль) получено из зависимости ушмренип СИ группы от температуры. Это значение но порядку величины соответствует числу кислых центров на поверхности у - Л12О3, определенных методом хроматографии. Малый парамагнетизм данного носителя позволяет исключить возможность адсорбции молекул на парамагнитных центрах. [9]
Величина 9 является функцией величины индивидуальных констант скоростей образования поверхностного комплекса и его превращения в десорбирующийся продукт и функцией давления реагирующего газа. [10]
Перенапряжение процесса ионизации металлов часто снижается в результате образования поверхностных комплексов с анионами электролита, причем образующийся комплекс гидратирован. [11]
По-видимому, механизм модифицирования поверхности Ni-катализатора заключается в образовании поверхностного комплекса никеля с модифицирующим веществом. [12]
Хотя основные результаты, по-видимому, свидетельствуют в пользу образования поверхностного комплекса С03, все же остается некоторое сомнение относительно точной роли кислородных ионов кристаллической решетки окислов. Винтер [17] показал, что при действии на обезгаженную закись никеля, приготовленную в виде окисной пленки на металле, кислорода, содержащего изотоп 180, при 540 происходит полный обмен всех поверхностных ионов кислорода окисла. Если после этого при температуре 200 производить напуск окиси углерода на окисел, содержащий теперь уже ионы 1802 -, то никакого заметного обмена кислорода не наблюдается. Аналогичным образом не происходит и обмен между кислородом С02 и ионами кислорода твердого окисла. Из этого следует, что, по-видимому, по крайней мере в случае N10 ионы кристаллической решетки окисла не принимают участия в реакции окисления СО, как это предполагается схемой Стоуна, описанной выше. [13]
Снижение перенапряжения процесса растворения - выделения металла часто происходит в результате образования поверхностных комплексов с анионами раствора электролита. Как мы видели, ионы хлора в щелочных растворах депас-сивируют железо. Галоиды оказывают активирующее действие, адсорбируясь в виде ионов, причем образующийся комплекс, очевидно, гидратирован. Вероятно, во многих случаях такого рода активация может быть объяснена на основании теории двойного слоя при учете г) 1-потенциала. Гидратированнын поверхностный комплекс металла с галоидом легко теряет связь с основной массой металла и переходит в раствор. Пассивирующее действие аниона связано, вероятно, с более глубоким взаимодействием между анионом и металлом, приводящим к образованию поверхностных соединений, теряющих гидратирующую воду и получающих свойства пленки. [14]
Образование парных электронных связей между адсорбентом и адсорбируемой молекулой может привести к образованию поверхностных комплексов с простой ковалентной связью. Довольно часто конфигурация комплекса очевидна, например при адсорбции одновалентной частицы на ковалентно связанный поверхностный атом, имеющий один неспаренный электрон. Трудности возникают втом случае, когда можно постулировать целый ряд различных конфигураций, каждая из которых вполне допустима; в этом случае необходимо найти критерий выбора правильной конфигурации. В случае двухточечной связи адсорбированной частицы с поверхностью комплекс должен соответствовать параметрам кристаллической решетки, последнее приведет к эффекту деформации, который надо учитывать. [15]
Страницы: 1 2 3 4