Образование - поверхностный комплекс
Cтраница 3
Представление о роли поверхностного комплексообразования в гетерогенном катализе развивалось в двух направлениях: с одной стороны, сам акт адсорбции рассматривался как образование поверхностного комплекса, а с другой, после привития поверхности комплексных соединений выявлялись возможности и особенности проведения на поверхности реакций, протекающих по механизму гомогенного катализа с теми же комплексами. [31]
 |
Закрепление [ IMAGE ] Проникновение молекул. [32] |
Были получены данные, свидетельствующие о том, что катализ ионами никеля обусловлен адсорбцией этих ионов из раствора в количествах, достаточных для образования поверхностного комплекса. Одна молекула а-оксистеариновой кислоты связывается с одним ионом никеля, так что при протекании реакции с молекулами монослоя на поверхности концентрируются очень небольшие количества ионов металла. [33]
Детальный анализ работ [9,10], где рассмотрено образование НгОадс и ОНаДе ( или МеОНаДс), показал [13], что адсорбция воды с образованием поверхностных комплексов с переносом заряда ( ПКПЗ) может привести к электростатическому экранированию металла адсорбционным слоем и резкому снижению зависимости скорости электрохимической реакции от потенциала. [34]
Можно предположить, что образование таких ионов осуществляется в несколько стадий [16], первой из которых является активированная адсорбция кислорода воды, приводящая к образованию поверхностного комплекса. Эта стадия сменяется затем электрохимической - стадией перехода комплекса в раствор. Лимитирующей стадией всего процесса является, по-видимому, последняя стадия. [35]
Альтшулером и Чухановым [195] предлагается следующая схема механизма реакции C02 - j - C 2CO в виде последовательных стадий: адсорбции С02 на поверхности угля, образования поверхностного комплекса ( по нулевому порядку), термического разложения комплекса ( по нулевому порядку) и распада комплекса при ударе молекул С02 из газовой фазы, протекающего по первому порядку. [36]
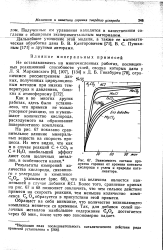 |
Зависимость состава продуктов горения от времени контакта кислорода с углем и природы катализатора. [37] |
Как и во многих других работах, здесь было установлено, что примеси не только ускоряют реакцию, но и уменьшают количество кислорода, расходуемого на образование поверхностного комплекса. [38]
Приведенные примеры убедительно показывают что на различных стадиях приготовления катализаторов а также под воздействием реакционной среды происходят как качественные так и количественные изменения состава поверхности: восстановление-окисле-кие образование поверхностных комплексов сплавов на носителях, обогащение или обеднение поверхности определенными компонентами. [39]
Различная степень неоднородности углерода и разное соотношение в нем пор обусловливают при контакте его с активными газами неодинаковую склонность к физической или химической адсорбции газов на поверхности углерода ( образование поверхностных комплексов), десорбирование которых приводит к повышению энергии поверхности углерода. [40]
С позиций механизма конкурентной сорбции, как стадии глубокого окисления влияние водяных паров можно объяснить тем, что молекулы воды, адсорбируясь на активных центрах катализатора, принимает участие в образовании поверхностных комплексов и влияют на их дальнейшее разложение. [41]
В работе [153] рассмотрена возможность применения следующих моделей для количественного описания адсорбции электролитов на активированных углях: электростатическая и специфическая адсорбция по Гун-Чапмену; сольватационная модель; ион-обменная модель; модель образования поверхностных комплексов. [42]
Перенос этой схемы на процесс горения в слое при температурах свыше 1000 С является не обоснованным, так как при высоких температурах, и условиях горения угля в слое хемадсорбционные процессы образования поверхностных комплексов не играют роли в общем ходе реакции. [43]
Роль энергетических и кинетических факторов, определяющих образование пленок, по-видимому, наиболее важна в тех случаях, когда в системе имеется более двух растворенных поверхностно-активных веществ, поскольку в таких системах наблюдается эффект пенетрации монослоев или образования поверхностных комплексов ( см. гл. Шульман и др. [16, 17] отмечают, в частности, что эмульсии особенно устойчивы, если адсорбированная пленка поверхностно-активного вещества образует прочные поверхностные комплексы с частицами масляной фазы. [44]
Процесс катализа на твердых пористых катализаторах складывается из следующих элементарных стадий: 1) диффузии реагирующих веществ из ядра потока к поверхности зерен катализатора; 2) диффузии реагентов в порах зерна катализатора; 3) активированной адсорбции ( хемосорбция) на поверхности катализатора с образованием поверхностных химических соединений - активированных комплексов: реагенты - катализатор; 4) перегруппировки атомов с образованием поверхностных комплексов: продукт - катализатор; 5) десорбции продукта с поверхности; 6) диффузии продукта в порах зерна катализатора; 7) диффузии продукта от поверхности зерна катализатора в ядро потока. [45]
Страницы: 1 2 3 4