Образование - активированный комплекс
Cтраница 1
Образование активированных комплексов на поверхности GaAs тесно связано с преобладанием ковалентиого характера связи у этого соединения. Тип гибридизации в комплексе может существенно измениться. Например, после ухода в раствор атомов мышьяка возникает существенное искажение тетраэдрической координации и, как следствие, изменение типа гибридизации орбита-лей. Подобное явление возникает для атомов Ga, связанных на поверхности GaAs. Изменение типа гибридизации значительно снижает энергию активации атомов Ga с мышьяковой поверхности типа В. Переход атомов Ga с галлиевой поверхности типа А соответствует значительно более высокой энергии активации, связанной с необходимостью разрыва 5р3 - гибридных связей. [1]
Образование активированного комплекса требует затраты энергии. Вероятность того, что при столкновении частиц образуется активированный комплекс и произойдет реакция, зависит от энергии сталкивающихся частиц. Реагируют только те из молекул, энергия которых для этого достаточна. Такие молекулы называют активными. [2]
Образование активированного комплекса способствует быстрому протеканию радиоактивного обмена между этими двумя ионами. Обмен заключается в переносе мостикового атома водорода з переходном состоянии. Расстояния Fe-О в соединениях Fe ( II) и Fe ( III) равны 2 21 и 2 05 А соответственно. [3]
Образование активированного комплекса в каждой реакции требует определенной энергии активации, распад же его происходит самопроизвольно. [4]
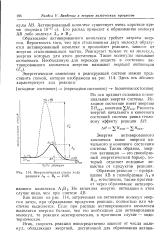 |
Энергетическая схема хода реакции А2 - f В2 2АВ. [5] |
Образование активированного комплекса требует затраты энергии. Вероятность того, что при столкновении двух молекул образуется активированный комплекс и произойдет реакция, зависит от энергии сталкивающихся частиц. Реагируют только те из молекул, энергия которых для этого достаточна. Такие молекулы называют активными. [6]
 |
Зависимость константы скорости распада иона от его внутренней энергии. [7] |
Образование активированного комплекса ( переходного состояния), который может привести к распаду, зависит от того, какое количество внутренней энергии сконцентрировалось вдоль координаты реакции. Так, если реакция представляет собой простой разрыв св язи, то на этой связи должна сконцентрироваться энергия, равная энергии разрыва этой связи. Очевидно, что если общая внутренняя энергия иона меньше энергии, необходимой для разрыва связи, то скорость реакции будет равна нулю. Если внутренняя энергия иона больше пороговой, то вероятность того, что требуемая энергия будет сосредоточена на данной связи, тем больше, чем больше эта внутренняя энергия. [8]
Образование активированного комплекса подчиняется обычным соотношениям кинетики. [9]
Образование активированного комплекса сопровождается изменением изобарного потенциала, и, следовательно, теплосодержания и энтропии. [10]
Поэтому образование активированного комплекса характерно для подавляющего большинства процессов. [11]
Для образования активированного комплекса во внутримолекулярной реакции гидролиза монофениловых эфиров дикарбоно-вых кислот необходимо, чтобы молекулы воды, гидролизующие заряженную карбоксилатную группу, были удалены. Рассмотрение молекулярных моделей показывает, что эта группа в сложном эфире V ( с. Поэтому при протекании данной внутримолекулярной реакции энергия для удаления воды в этом положении из гидратной оболочки не требуется. [12]
Поэтому образование активированного комплекса характерно для подавляющего большинства процессов. [13]
 |
Орбитали атома Н и моле - [ IMAGE ] Орбитали иона ОН - и молекулы С12, участвующие в реакции ( III кулы СН31, участвующие в реакции ( I. [14] |
Поэтому образование активированного комплекса происходит легко и протекание реакции связано с преодолением невысокого энергетического барьера. [15]
Страницы: 1 2 3 4