Образование - активированный комплекс
Cтраница 3
В гемолитических реакциях образование активированных комплексов не сопровождается значительным перераспределением электрических зарядов между реагирующими частицами. Следовательно, при этих реакциях не происходит существенного изменения межмолекулярных взаимодействии реагирующих частиц с молекулами растворителя, скорость реакции мало зависит от природы растворителя. [31]
В некоторых реакциях образование активированного комплекса сопровождается освобождением других молекул или ионов, которые не принимают больше участия в реакции. Например, при реакции между веществами А и В, наряду с образованием активированного комплекса Л / fi, могут образоваться устойчивые вещества N и О. [32]
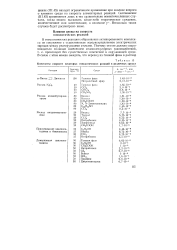 |
Константы скорости некоторых гомолитических реакций в различных средах. [33] |
В гемолитических реакциях образование активированного комплекса не сопряжено с существенным перераспределением электрических зарядов между реагирующими атомами. [34]
Таким образом, образование активированного комплекса требует затраты энергии. Для прохождения реакции должен быть преодолен некоторый энергетический барьер; его наличием и обусловлена возможность существования смесей веществ в течение длительного времени, несмотря на уменьшение G при их взаимодействии. [35]
Поэтому сам факт образования активированного комплекса и служит необходимым условием осуществления данного элементарного акта. Активированный комплекс образуется и разлагается, превращаясь в продукты реакции в одном элементарном акте ( в элементарной стадии), и в этом заключается коренное отличие активированных комплексов от промежуточных соединений помимо того, что последние могут быть обнаружены. Действительно, промежуточные соединения, образовавшись, могут превращаться либо в продукты реакции, либо вновь в исходные вещества. Активированный комплекс лишен такого права выбора, образовавшись, он переходит в другие промежуточные состояния только в направлении перехода в продукты реакции. Образование и разложение промежуточных соединений представляет собой, по крайней мере, два элементарных процесса, каждому из которых присущ свой активированный комплекс. [36]
Чтобы определить скорость образования активированных комплексов и, следовательно, скорость реакции, необходимо проинтегрировать вероятность ( Е - E0) dn по всем энергиям от Е0 до бесконечности. Однако поскольку ничего неизвестно о распределении энергии в неравновесных условиях или о величине п для высоких значений энергии Е - то количественных результатов получить не удается, если только не вводить новых предположений. [37]
На энергии активации образования активированного комплекса непосредственно сказываются энергии трансформирующихся при реакции связей. [38]
Изменение объема при образовании активированного комплекса также встречает сопротивление со стороны решетки. Изменение свободной энергии, которое при этом происходит, можно грубо оценить на основе макроскопических представлений. [39]
Изменение объема при образовании активированного комплекса также встречает сопротивление со стороны решетки. При этом оказывается, что энергия активации реакции возрастает с ростом изменения объема при образовании активированного комплекса. [40]
Переходное состояние 4 Возможно образование активированного комплекса. [41]
Равновесие быстро установится через образование внешне-сферных активированных комплексов, и радиоактивный марганец будет распределен между двумя степенями окисления точно в том же соотношении, что и нерадиоактивный марганец. [42]
Равновесие быстро установится через образование внешне-сферных активированных комплексов, и радиоактивный марганец будет распределен между двумя степенями окисления точно в том же соотно-шении, что и нерадиоактивный марганец. [43]
К - константа равновесия образования активированного комплекса; С0 - стандартная величина, выбранная для концентрации газа. [44]
При совместном рассмотрении процессов образования активированных комплексов, их превращения в активную частицу-продукт и ударной стабилизации последней необходимо учесть также возможность дезактивации активных частиц при соударениях. Кроме того, следует учесть, что активация частиц реагентов, дезактивация активных частиц и стабилизация активных частиц-продуктов может происходить с участием любых частиц, присутствующих в реакционной смеси. При написании процессов обмена энергией не будет делаться различий в обозначении частицы М до и после обмена энергией, хотя, естественно, энергия этой частицы изменяется - возрастает в процессах дезактивации и стабилизации и уменьшается в процессе активации. [45]
Страницы: 1 2 3 4