Образование - активный комплекс
Cтраница 3
Наличие заряда на кислороде может благоприятствовать образованию активного комплекса, приводящего к изотактической форме. Естественно, что стереорегулирующее действие катализатора должно зависеть от структуры противоиона, в частности от его радиуса. [31]
Такой механизм в его первой стадии ( образование активного комплекса) вполне аналогичен реакции образования аммонийного иона лз молекулы амина при присоединении к ней протона. [32]
 |
Энтальпийная диаграмма реакций некаталитической A BD и с участием катализаторов К и К. [33] |
К каталитическим реакциям, проходящим через стадию образования активного комплекса, приложимы кинетические закономерности, используемые в теории переходного состояния. Скорость образования активного комплекса выше скорости его распада на продукты и катализатор, поэтому скорость процессов в целом определяется скоростью распада активного комплекса. Скорость реакции прямо пропорциональна концентрации катализ-атора. [34]
Совокупность атомов реагирующих веществ, участвующих в образовании мультиплетного активного комплекса, называется индексом данного типа реакций. [35]
 |
Энергетическая диаграмма взаимодействия H2 l2. t2HI. [36] |
Квантовомеханические расчеты показывают, что протекание реакции через образование активного комплекса энергетически выгоднее, чем возникновение новых связей после полной диссоциации исходных компонентов. [37]
Как было показано в § 20, процессы образования активного комплекса в жидких фазах могут быть выражены в терминах химических реакций. Поскольку речь идет о неравновесном состоянии, степени полноты этих реакций 0 представляют собой внутренние переменные, определяющие состояние неравновесной системы. Подчеркнем, что реакция q не обязательно должна входить в перечень реакций, обозначаемых здесь и далее индексом а. Например, реакции а могут быть быстрыми и сверхбыстрыми, а реакция q - медленной. [38]
Присутствие солей других элементов влияет на равновесие реакции образования активного комплекса. Такое влияние называют обычно солевым эффектом первого рода. [39]
Здесь точками показаны только связи, возникшие при образовании активного комплекса. Рвущиеся связи перечеркнуты пунктиром. [40]
Это выражение применимо к любой реакции, протекающей через образование активного комплекса. [41]
К изложенному выше следует добавить, что в пользу образования активного комплекса ( без возникновения кинетически независимых нейтральных частиц) при течении так называемых свободно-радикальных реакций, свидетельствует также низкая ( иногда даже комнатная) температура, при которой идут эти реакции. [42]
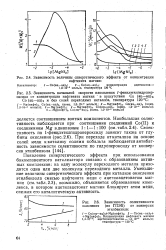 |
Зависимость величины синергетического эффекта от концентрации.| Зависимость начальной скорости накопления / - фенилэтилгидропер. [43] |
Появление синергетического эффекта при использовании бикомпонентного катализатора связано с образованием активных комплексов: на одну молекулу переходного металла приходится одна или две молекулы переходного металла. Уменьшение величины синергетического эффекта при катализе окисления этилбензола смесью нафтената меди с ацетилацетонатом магния ( см. табл. 2.3), возможно, объясняется образованием комплекса, в котором ацетилацетонат магния блокирует атом меди, снижая его каталитическую активность. [44]
На атомах металла в октаэдрических катионных узлах более благоприятны условия для образования активного комплекса с симметрией С6 ( ось вращения 6-го порядка), которая соответствует симметрии бензольного кольца в образующемся толуоле. В других реакциях преимущества оксида алюминия перед силикагелем могут быть менее существенны. [45]
Страницы: 1 2 3 4