Образование - л-связь
Cтраница 2
Влияние ковалентности и образования л-связей в связи металл - лиганд на энергии заполненных и пустых орбиталей также лучше всего описывается методом молекулярных орбита-лей. [16]
 |
Структуры молекулы анилина. [17] |
Поэтому приводящее к образованию л-связи перекрывание / з-орбитали атома углерода и почти тетраэдрической гибридной АО неподеленной пары атома азота будет не очень значительным. Резонансные и обменные интегралы между С и N должны быть меньше, и соответственно меньшими будут веса ионных структур, изображенных на рис. 9.13, б, в. Тем не менее можно утверждать, что 1) резонансный момент молекулы должен быть таким, чтобы электроны передавались кольцу и на атоме азота оставался небольшой положительный заряд, и 2) структуры, в которых избыток заряда кольца находится на атомах мета-углерод а, энергетически гораздо менее важны, чем структуры б и в, в которых этот избыток находится на атомах орто - и яара-углерода. [18]
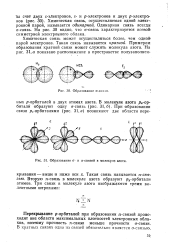 |
Образование а-связи.| Образование а - и я-связей в молекуле, азэда. [19] |
Перекрывание р-орбиталей при образовании л-связей происходит вне области максимальных плотностей электронных облаков, поэтому прочность л-овяэи меньше прочности а-связи. [20]
 |
Стереохимия соединений S, Se, Те. [21] |
Конечно, можно объяснить образование л-связей в SO2, не используя d - орбиталь серы, а рассматривая эту молекулу, как нитро-группу. При этом в образование молекулярных л-орбита-лей вносят вклад атомная Зр2 - орбиталь серы и 2р2 - орбитали кислорода; возникает заполненная делокализованная связывающая молекулярная л-орбиталь и заполненная несвязывающая л-орби-таль, локализованная только на двух атомах кислорода. [22]
 |
Схема перекрывания t2s ( dxy - орбитали центрального атома с sg ( p - групповыми орбиталями лигандов в плоскости ху. [23] |
Таким образом, для образования л-связей остаются орбитали Г2г - сим-метрии. [24]
Если допустить, что образование дополнительной л-связи между реакционным центром и заместителями у четырехкоординационного атома фосфора приводит, кроме изменений энергий связи, также и к изменению энергии внутреннего вращения молекулы, то это скажется на изменении вращательной суммы состояний, а следовательно, и на полной сумме состояний, что найдет отражение в изменении величин F и FA. При этом, по-видимому, изменение в случае F и F будет неравноценным, так как сопряжение заместителей с реакционным центром значительно усиливается в переходном состоянии по сравнению с основным состоянием молекул ( см. также стр. И, следовательно, величина F уменьшается в большей степени, чем FA, что должно в свою очередь привести к снижению константы скорости реакции. [25]
В целом же вероятность образования л-связи двумя любыми соседними атомами С вдвое меньше, чем у этилена, то есть бензольная я-связь перекидывается над всем периметром молекулы и должна быть - в д в о е слабее этиленовой тс-связи: согласно расчету, энергия л-связи в бензоле и составляет ( 88 - 62 7) 23 3 ккал / моль. Вывод: двойная бензольная связь - промежуточная по характеру между двойной этиленовой одинарной; она и сообщает бензолу свойства промежуточные между свойствами предельных и этиленовых углеводородов ( способность и к реакциям замещения и к реакциям присоединения) и требует иных способов ее графического изображения. [26]
В целом же вероятность образования л-связи двумя любыми соседними атомами С вдвое меньше, чем у этилена, то есть бензольная тс-связь непрерывно перемещается перпендикулярно плоскости по всему периметру молекулы. В результате двойная бензольная связь - промежуточная по характеру между двойной этиленовой и одинарной; она и сообщает бензолу свойства, промежуточные между свойствами предельных и этиленовых углеводородов ( способность в основном к реакциям замещения и в меньшей степени к реакциям присоединения) и требует иных способов ее графического изображения. [27]
Рис, 11.56. Влияние образования л-связи на плотность заряда d - электрона. [28]
 |
Образование л-связей металла с лигандами. [29] |
В результате появляется возможность образования л-связей лигандов с центральным ионом за счет перекрывания dxy -, dX2 - и - орбиталей металла со свободными разрыхляющими орбиталями лигандов. Уровень tig при этом опускается вниз и становится связывающим, а энергия расщепления А увеличивается. Связь, образованную d - электронами центрального иона и свободными орбиталями лигандов, называют дативной. [30]
Страницы: 1 2 3 4 5