Образование - л-связь
Cтраница 3
Электроны, участвующие в образовании л-связей. [31]
Молекулярные орбитали, возникающие при образовании а-и л-связей между различными элементами, обычно не симметричны относительно атомных ядер, так как одни атомы притягивают электроны сильнее, чем другие. [32]
 |
Перекрывание 25-орбитали атома кислорода с ls - орбиталями атомов водорода. [33] |
Отметим, что 2ри пригодна для образования л-связи, однако атомы водорода не имеют валентных л-орбиталей. [34]
 |
Схематическое изображение латерального связывания двух р-орбит. [35] |
Наоборот, электроны, участвующие в образовании л-связей ( обычно называемые it - электронами), локализованы в меньшей степени. Малая степень локализации jt - связей подтверждается, в частности, большой поляризуемостью этих связей ( стр. [36]
К числу соединений, в которых возможно образование & л-связей, принадлежат все производные фосфора типа X PY3, в том числе фосфазосоединения. [37]
Уменьшение длины связей в циклотриборазенах может быть обусловлено образованием л-связей, сообщающих кольцу ароматический характер. [38]
Атомные s - орбитали не принимают участия в образовании л-связи. [39]
Кроме того, трансактивный лиганд обычно участвует в образовании дативной л-связи с комплексообразователем, оттягивая на себя его d - электроны. В результате в пространстве за комплексообразователем электронная плотность понижается, и лиганд, находящийся в транс-положении, легче подвергается атаке частицы какого-либо реагента. Это проявляется в повышении реакционной способности комплекса, в увеличении скорости замещения траяс-лиганда. [40]
Кроме того, транс-активный лиганд обычно участвует в образовании дативной л-связи с комплексообразователем, оттягивая на себя его d - электроны. В результате в пространстве за комплексообразователем электронная плотность понижается и лиганд, находящийся в транс-положении, легче подвергается атаке частицы какого-либо реагента. Это проявляется в повышении реакционной способности комплекса, в увеличении скорости замещения транс-лиганда. [41]
Теория л-связей, предложенная Чаттом и Оргелом, учитывает образование ковалентной л-связи в качестве одного из наиболее важных факторов и подчеркивает увеличение стабильности переходного состояния в реакциях замещения, протекающих по ассоциативному механизму, обусловленное наличием л-связи. [42]
Могут ли s - орбитали соседних атомов быть причиной образования л-связи между этими атомами. [43]
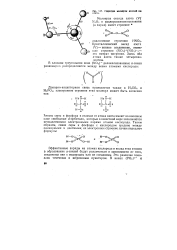 |
Структура молекулы азотной ки. [44] |
Эффективные заряды на атомах кислорода и вклад этих атомов в образование л-связей будут различаться в зависимости от того, соединены они с водородом или не соединены. Это различие показано точечным и штриховым пунктиром. [45]
Страницы: 1 2 3 4 5