Образование - гальванические пары
Cтраница 1
Образование гальванических пар в металлах и сплавах может носить самопроизвольный характер и быть источником коррозии. [1]
 |
Механизм химической ( д и электрохимической ( б коррозии. [2] |
Роль образования гальванических пар в процессе взаимодействия с электролитом может быть выяснена на таком примере. Известно, что ни медь, ни серебро не вытесняют водород из кислот, но если в раствор соляной ( хлороводородной) кислоты опустить соединенные проводником пластины из меди и серебра ( коротко-замкнутый гальванический элемент), то происходит выделение водорода. [3]
Причиной образования местных гальванических пар в принципе являются так называемые местные неоднородности. [4]
Важно избегать образования гальванических пар алюминия со сталью или сплавами на основе меди. Описаны методы уменьшения питтинговой коррозии с помощью входных фильтров и ловушек, задерживающих ионы тяжелых металлов. Прекрасная коррозионная стойкость, низкая стоимость и хорошая обрабатываемость делают алюминиевые сплавы наиболее удобным материалом для изготовления оборудования опреснительных установок. [5]
Это обусловливает образование короткозамкнутых гальванических пар. [6]
По новым представлениям образование гальванических пар вызывается очень многими причинами. [7]
В некоторых случаях образование гальванических пар дает положительный эффект. Например, питтинговая и общая коррозия алюминиевых сплавов уменьшается при их соединении с алюминиевыми или цинковыми анодами. Аноды из магния применять не следует, так как более высокий потенциал приведет к перезащите и повышению рН среды около катода. [8]
Объяснить, как влияет образование гальванических пар на коррозию металлов. [9]
 |
Кривые плотность тока - потенциал при контактной коррозии. [10] |
Таким образом, для образования местных гальванических пар характерны неоднородный потенциал металла и пространственно разделенные строго локализированные анодные и катодные участки на поверхности металла. В результате наблюдается неравномерный съем металла с поверхности. [11]
При сопряжении деталей не допускается образование гальванических пар, вызывающих коррозию металла, особенно, если сопряженные детали будут работать при повышенной влажности воздуха. В табл. 21.6 приведены недопустимые гальванические пары. [12]
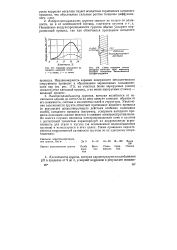 |
Влияние влажности на скорость коррозии стали. / - в песке. 2 - в глине.| Схема коррозии стенок обсадных стальных труб нефтяных скважин вследствие биологической сульфат-редукции. [13] |
Неравномерность аэрации поверхности металлического сооружения приводит к образованию аэрационных гальванических пар ( см. рис. 171): на участках более аэрируемых ( песок) локализуется катодный процесс, а на менее аэрируемых ( глина) - анодный процесс. [14]
При выборе материала металлических защитных покрытий стремятся не допустить образования гальванических пар, вызывающих коррозию основного металла детали. [15]
Страницы: 1 2 3 4