Образование - пероксид - водород
Cтраница 3
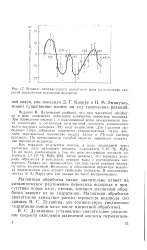 |
Влияние напряженности магнитного поля на изменение скорости разложения псрокснда водорода. [31] |
Автор полагает, что пероксид водорода образуется в результате реакции воды с растворенным кислородом. Однако это маловероятно, так как такая реакция является очень энергоемкой. Возможно, в образовании пероксида водорода определенную роль играют свободные радикалы. В аналогичных опытах Э. А. Маргулиса эти данные не были воспроизведены. [32]
Процесс состоит из двух основных стадий. Перок-сид водорода экстрагируют водой из органического растворителя и, при необходимости, концентрируют. В конечном итоге процесс сводится к образованию пероксида водорода из водорода и кислорода, остальные реагенты циркулируют почти неизменными. [33]
При замене одного атома водорода в молекуле Н2С2 на атом металла получаем надоснования, например К - О-О - ОН. Поскольку подобные соединения можно рассматривать как кислые соли пероксида водорода, их часто именуют гидро-пероксидами. Характерное свойство пероксидов металлов, пероксокислот и гид-ропероксидов - способность подвергаться гидролизу с образованием пероксида водорода и разлагаться, выделяя кислород, т.е. быть окислителями. [34]
Было показано, что пе-роксодвусерная кислота гидролизуется с образованием кислоты Каро, а последняя гидролизуется с образованием пероксида водорода. Одной из причин разложения является наличие в растворе примесей катализаторов. [35]
Как показывает опыт, удаление из воды микроводорослей приводит к резкому снижению скорости разложения пероксида водорода, тогда как введение в природную воду концентрата водорослей из того же водоема приводит к значительному возрастанию скорости. Введение в такую химико-биологическую систему Н2О2 - микроводоросли - примеси ионов переходных металлов) загрязняющих веществ сопровождается их быстрым окислением за счет ОН радикалов, возникающих при распаде пероксида водорода. Результаты этих исследований позволили предложить редокс-модель природной воды, согласно которой микроводорослевая биота участвует как в образовании пероксида водорода под действием солнечного света, так и в ее разрушении за счет выделения во внешнюю среду веществ с ярко выраженными восстановительными свойствами. [36]
Имеются указания на образование пероксида водорода при восстановлении атмосферного кислорода. Бердик [83] утверждает, что пероксид образуется только в том случае, если вместо кислоты в цинковом редукторе в качестве растворителя используют воду. Действительно, Лендел и Ноулз [84] показали, что пероксид полностью разрушается при восстановлении кислорода цинком в кислом растворе. Вместе с тем, Силл и Петерсон [85] обнаруживали образование пероксида водорода при быстром пропускании пузырьков воздуха через колонку с сильно амальгамированным цинком. При использовании свинцового редуктора образуются значительно большие количества пероксида. [37]
Страницы: 1 2 3