Образование - новая ковалентная связь
Cтраница 2
Реакциями электрофильного замещения называются такие реакции, при которых бедный электронами атакующий реагент присоединяет к себе пару электронов от атакуемого компонента с образованием новой ковалентной связи. Электрофильными реагентами являются положительно заряженные ионы Н, No и все нейтральные молекулы, в состав которых входят атомы с недоукомплектованными электронными орбиталями. [16]
Швенкер и др. [38] кратко описали процесс термодеструкции тозилатов, мезилатов и других сложных эфиров целлюлозы, заключающийся в отщеплении кислотных групп и образовании новых ковалентных связей. [17]
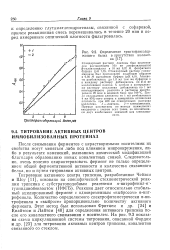 |
Определение триптофансодер-жащего белка в присутствии коллагена. [18] |
После связывания ферментов с нерастворимыми носителями их свойства могут меняться либо под влиянием микроокружения, либо в результате изменений, вызванных химической модификацией благодаря образованию новых ковалентных связей. Следовательно, очень полезно охарактеризовать фермент не только определением общей ферментативной активности и количества связанного белка, но и путем титрования активных центров. [19]
Первый тип реакции ( Syi) сопровождается образованием конечного продукта ( ВС) и промежуточной заряженной частицы - аниона, а второй ( 5к) - того же продукта ( ВС) и катиона. Реагент, который предоставляет электронную пару для образования новой ковалентной связи, называется нуклеофильным, или электронодонорным. [20]
Важно учитывать существование и межмолекулярных взаимодействий в органических соединениях. Речь идет о взаимодействиях, которые не сопровождаются образованием новых ковалентных связей, но определяют силы притяжения между молекулами, а тем самым - фазовое состояние и физические свойства органических соединений. Эти силы притяжения имеют электрическую природу и обусловлены следующими составляющими. [21]
Эти реакции обмена ( экзотермические или слабо эндотермические) характеризуются крайне малыми энергиями активации ( 0 - 5 ккал / молъ) и, следовательно, очень большими скоростями. Объяснение этого факта вытекает именно из механизма переходного состояния: энергия, выделяющаяся при образовании новой ковалентной связи, компенсирует энергию, израсходованную на разрыв исчезающей связи. [22]
Эти реакции обмена ( экзотермические или слабо эндотермические) характеризуются крайне малыми энергиями активации ( 0 - 5 ккал / молъ) и, следовательно, очень большими скоростями. Объяснение этого факта вытекает именно из механизма переходного состояния: энергия, выделяющаяся при образовании новой ковалентной связи, компенсирует энергию, израсходованную на разрыв исчезающей связи. [23]
Любой способ стабилизации ионов путем делокализации заряда, будь то за счет групп, входящих в состав иона или за счет сольватации, разумеется, тем эффективнее, чем значительнее смещение электронов к катионному центру или от анионного центра. Такая делокализация, однако, не должна переходить некоторые пределы, за которыми происходит разрыв старых или образование новых ковалентных связей. [24]
Любой способ стабилизации ионов путем делокализации заряда, будь то за счет групп, входящих в состав иона, или за счет сольватации, разумеется, тем эффективнее, чем значительнее смешение электронов к катионнму центру карбокатионов или от анионного центра карбанионов. Такая делокали-зация не должна, однако, переходить некоторые пределы, за которыми может произойти разрыв старых и / или образование новых ковалентных связей. Один подобный пример мы уже приводили: п mpem - бутильном катионе ( 26), стабилизация которого осуществляется за счет поляризации связей С - Н, 1гри неблагоприятных условиях может произойти полный сдвиг заряда, результатом чего будет выброс протона и образование двойной связи. [25]
Любой способ стабилизации ионов путем делокализации заряда, будь то за счет групп, входящих в состав иона, или за счет сольватации, разумеется, тем эффективнее, чем значительнее смешение электронов к катионнму центру кзрбокатионов или от анионного центра карбанионов. Такая делокали-зация не должна, однако, переходить некоторые пределы, за которыми может произойти разрыв старых и / или образование новых ковалентных связей. Один подобный пример мы уже приводили: в / и ет-бутильном катионе ( 26), стабилизация которого осуществляется за счет поляризации связей С - Н, при неблагоприятных условиях может произойти полный сдвиг заряда, результатом чего будет выброс протона и образование двойной связи. [26]
Любой способ стабилизации ионов путем делокализации заряда, будь то за счет групп, входящих в состав иона, или за счет сольватации, разумеется, тем эффективнее, чем значительнее смещение электронов к катионнму центру карбокатионов или от анионного центра карбанионов. Такая делокали-зация не должна, однако, переходить некоторые пределы, за которыми может произойти разрыв старых и / или образование новых ковалентных связей. Один подобный пример мы уже приводили: в трет-бупшъном катионе ( 26), стабилизация которого осуществляется за счет поляризации связей С - Н, при неблагоприятных условиях может произойти полный сдвиг заряда, результатом чего будет выброс протона и образование двойной связи. [27]
Если в полифункциональном структурирующем агенте утеряна одна из функций вследствие гидролиза, то связь может легко образовываться за счет других функций. Более того, гидролиз мостиковой группы приводит к образованию соединений, имеющих нук-леофильный характер и способных, в свою очередь, вступать в реакцию. Предположение об образовании новой ковалентной связи было проверено с помощью обычных для активных красителей методов. В качестве структурирующих агентов применяли соединения, содержащие не менее двух положительно поляризованных С-атомов. В соответствии со свойствами активных красителей структурирующие агенты можно разделить на три группы: соединения, которые реагируют за счет присоединения к активированным двойным связям; соединения, реагирующие по механизму замещения и соединения, реагирующие по механизму конденсации. Веглером и Баллауфом - [220], и легко доступен. Структурирующие агенты, которые могут подвергнуться катализу в кислой или щелочной среде, например при проведении противосминаемой отделки целлюлозных тканей, применять для связывания красителя с волокном нельзя. Соединения типа динатриевой соли трис - ( р-сульфоксиэтил) сульфония, возможно, способны вступать в реакцию с целлюлозой, но с красителями они могут реагировать только ограниченно. Соединения, которые, кроме структурирования, создают еще и эффект несминаемости, применять нельзя, так как под их действием некоторые участки волокна становятся настолько жесткими, что это может сказаться на общем качестве ткани. По данным Лютцеля [216, 218, 219], красители, которые можно фиксировать с помощью структурирующих агентов, должны содержать первичные или вторичные аминогруппы, сульфамидные, гидроксильные или меркаптогруппы, а также активные метилено-вые или NH-группы в гетероциклических системах. [28]
Присоединение фермента к субстрату обычно протекает наиболее быстро. Данная стадия имеет очень небольшую энергию активации и это показывает, что первичный комплекс ES образуется за счет слабых связей - гидрофобных, водородных и электростатических. Второй этап требует сравнительно много энергии - он связан с разрывом и затем образованием новых ковалентных связей. Суммарная скорость ферментной реакции определяется прохождением через ту стадию второго этапа, которая имеет наибольшую свободную энергию, иными словами, наиболее высокий энергетический барьер. Чем этот барьер выше ( и выше энергия активации этой стадии), тем труднее протекает каталитический процесс. Сказанное иллюстрируется рис. 13, где видны энергетический барьер реакции, идущей без катализатора; энергетические барьеры отдельных стадий при последовательных превращениях промежуточного комплекса фермент-субстрат и наиболее высокий из этих барьеров, лимитирующий скорость всего процесса. [29]
Любая классификация только приближенно отражает явления природы. Не служит исключением и описанная выше классификация реагентов. В ней предусматривается либо полный переход электронов от одного атома к другому, либо образование новой ковалентной связи между двумя атомами путем объединения электронной пары одного из них, хотя кроме гете-рополярных ( ионных, электровалентных) и гомеополярных ( молекулярных, ковалентных) связей существуют связи переходного типа. Ведь даже в ионных кристаллах нельзя полностью пренебречь существованием обменных сил, а в органических молекулах валентные связи более или менее полярны. [30]
Страницы: 1 2 3