Образование - сг-связь
Cтраница 1
 |
Взаимное перекрывание орбиталей атомов А и В с образованием а-связей А В А в А В.| Перекрывание орбиталей атомов А и В с образованием я-связей. [1] |
Образование сг-связи объясняется перекрыванием волновых функций электронов в одной области пространства, расположенной на оси ( обозначим ее через х), соединяющей центры взаимодействующих атомов. [2]
 |
Структура графита. [3] |
В образовании сг-связей участвуют три электрона каждого атома углерода. Четвертый электрон внешнего слоя занимает 2р - орби-таль, не участвующую в гибридизации. [4]
 |
Различные типы 7Г - связей и ( Т - свяэь. [5] |
В образовании сг-связей между углеродом и атомами водорода со стороны углеродных атомов участвуют р2 - орбитали, а водородных атомов - s - орбитали. [6]
 |
Схема строения молекулы бутадиена. [7] |
Каждый из атомов после образования обычной сг-связи имеет еще один р-электрон, который может принять участие в образовании л-связи путем бокового перекрывания. Таким образом, в сопряженной системе бутадиена л-электронная плотность не закреплена в определенных связях, а распределена по всей системе. [8]
В клетке растворителя могут рекомбинировать с образованием сг-связи только радикальные пары с антипараллельными спинами. Радикальные пары с параллельными спинами могут рекомбинировать в клетке только после инверсии спина, что возможно, например, у долгоживущих радикалов в вязких средах, препятствующих диффузии. В противном случае рекомбинация происходит только после диффузии из клетки растворителя. [9]
Атом X использует две гибридные sp - орбитали для образования сг-связей с атомами А и В. Кроме того, у него остаются еще две р-орбитали, расположенные под прямым углом в плоскости, перпендикулярной оси АХВ, которые могут комбинировать с соответствующими орби-талями А и В с образованием л-связей. Это показано на рис. 15.3. В каждом случае можно также предсказать высокий барьер внутреннего вращения А относительно В. [10]
В случае, когда 8 лигандов располагаются в вершинах куба и предполагается образование сг-связей, необходимо сформировать 8 МО. [11]
Если считать, что переход электронов лигандов на орбитали центрального иона сопровождается образованием координационной сг-связи, то обратный переход электронов с заполненных d - орбиталей центрального иона на разрыхляющие орбитали лигандов приводит к образованию, координационной п-связи. [12]
Для этих элементов характерно также участие d - орбиталей не только в образовании сг-связей, но и в формировании я-свя-зей. [13]
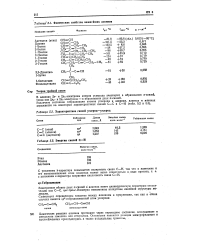 |
Физические свойства важнейших алкинов.| Характеристика связей углерод-углерод.| Энергия связей С - Н. [14] |
В алкинах 2s - и 2рх - электроны атомов углерода участвуют в образовании сг-связей, тогда как 2р - и 2рг - электроны - в Образовании двух я-связей. [15]
Страницы: 1 2 3