Образование - двойное соединение
Cтраница 1
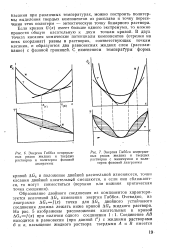 |
Энергия Гиббса непрерывных рядов жидких и твердых растворов и политерма фазовой диаграммы.| Энергия Гиббса непрерывных рядов жидких и твердых растворов с минимумом и политерма фазовой диаграммы. [1] |
Образование двойного соединения из компонентов характеризуется величиной АС изменения энергии Гиббса. Очевидно, на диаграмме & Gxf ( x) точка для ДОЖ двойного устойчивого соединения должна лежать ниже кривой AGK жидкого раствора. [2]
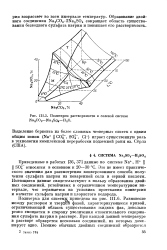 |
Политерма растворимости в солевой системе Na2CO3 - Na2S ( 4 - Н20. [3] |
Образование двойного соединения Na2C03 - 2Na2S04 сокращает область существования безводного сульфата натрия и повышает его растворимость. [4]
Образование двойного соединения в тройной системе, изображаемой в пространстве, характеризуется плоскостью состава этого соединения. Кривая, образуемая пересечением вдоль этой плоскости поверхностей кристаллизации компонентов, не может быть сингулярной. [5]
Образование двойных соединений между компонентами системы вызывает дополнительные разбиения стабильных тетраэдров. [6]
Обнаружено образование двойного соединения 1 10-фенантролина с хлороформом и установлен его состав. [7]
Им изучено образование ранее неизвестных двойных соединений 1 10-фенантролина с хлороформом. [8]
Во второй системе обнаружено образование двойных соединений. [9]
Общее свойство сульфидов - образование двойных соединений с солями тяжелых металлов за счет ненасыщенное серы - сохраняется и у иприта; так например: PtQ4, PtCla, AuCls, соли ртути ( HgCl2, Hgjj и меди образуют кристаллические молекулярные соединения с ипритом, нерастворимые в воде. [10]
Уже этот факт свидетельствует об образовании двойного соединения в растворе. Для приготовления Рис - 1-двойной платиновой соли поступают следующим образом. В 50 см. воды растворяют 13 г платотетрамминового хлорида; при нагревании этого раствора вносят постепенно 4 г хлористой соли второго основания и кипятят до полного растворения. Профильтрованный через горячий фильтр раствор медленно охлаждается на водяной бане, причем получают 7 5 г двойного соединения в виде коротких табличек буровато-желтого цвета. Из маточного раствора выпариванием до одной трети удается получить еще до 4 г этого вещества. Дальнейшее сгущение приводит к кристаллизации смеси двойной соли с бурыми призмами платинотетрамминоврго хлорида. Из крепкого раствора последнего вещества двойное соединение может быть перекристаллизовано без изменения. [11]
С увеличением радиуса иона возрастает энергия образования двойных соединений и повышается температура их плавления. [12]
Применение фтористого серебра невыгодно, потому что вследствие образования двойного соединения AgF AgX в реакции обмена участвует только половина наличного фтора и приходится брать два эквивалента фтористого серебра. При реакциях с высшими бромистыми алкилами иногда происходит отщепление бромистого водорода и образуется олефин. Образование при этой реакции олефина подтверждается тем, что при действии фтористого серебра на - бутилбромид наряду с н-бутилфторидом получается вгор. [13]
Способность этих углеводородов к реакциям присоединения проявляется также в образовании двойных соединений с некоторыми полинитросоединениями и с хинонами. [14]
Как цианид, так и роданид свинца обладают тенденцией к образованию двойных соединений с галогенидами свинца. [15]
Страницы: 1 2 3 4