Образование - перекисное соединение
Cтраница 2
В некоторых случаях образование перекисных соединений происходит мимолетно и существующими методами обнаруживается с трудом. Это относится прежде всего к низшим алкильным перекисям или гидроперекисям, скорость распада которых в процессе окисления зачастую очень велика. В других процессах, например, при окислении вторичных спиртов, скорость образования промежуточных перекисных соединений в определенных пределах их концентрации выше скорости их разложения, что приводит к накоплению их в реакционной смеси. Следовательно, получение их в качестве целевого продукта делается реальным, хотя и требует очень тщательного соблюдения условий, обеспечивающих селективность процесса и хороший выход перекисей. [16]
В некоторых случаях образование перекисных соединений происходит мимолетно и существующими методами обнаруживается, с трудом. Это относится прежде всего к низшим алкнльным перекисям или гидроперекисям, скорость распада которых в процессе окисления зачастую очень велика. В других процессах, например, при окислении вторичных спиртов, скорость образования промежуточных перекисных соединений в определенных пределах их концентрации выше скорости их разложения, что приводит к накоплению их в реакционной смеси. Следовательно, получение их в качестве целевого продукта делается реальным, хотя и требует очень тщательного соблюдения условий, обеспечивающих селективность процесса и хороший выход перекисей. [17]
Неудобством электролитического восстановления является образование перекисных соединений, часто искажающих результат титрования. Требующаяся для восстановления аппаратура в основном совпадает с аппаратурой, описанной в разделе Электролитические методы отделения ( стр. [18]
ТЭС мало влияет на образование перекисных соединений и реакции окисления углеводородов в начальной стадии и вызывает разрушение перекисей, ведущих к горячему взрыву. [19]
Неудобством электролитического восстановления является образование перекисных соединений, часто искажающих результат титрования. Требующаяся для восстановления аппаратура в основном совпадает с аппаратурой, описанной в разделе Электролитические методы отделения ( стр. [20]
ТЭС мало влияет на образование перекисных соединений и реакции окисления углеводородов в начальной стадии и вызывает разрушение перекисей, ведущих к горячему взрыву. [21]
В процессе метаболизма происходит образование перекисных соединений, фтороводорода, возможно образование щавелевой кислоты. Дефторирование протекает относительно медленно. [22]
Окисление толуола идет через образование промежуточного перекисного соединения с последующим распадом на альдегид и воду. [23]
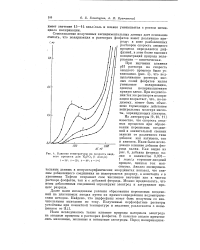 |
Влияние температуры на скорость анодного процесса для К3Р04 ( 1 моль / л г - 35. 3 - 25. 3 - 18. 4 - 5 С. [24] |
Далее нами исследованы условия образования перекисных соединений на платиновых анодах путем их прямого определения иодометриче-ским методом. Найдено, что перфосфаты могут быть получены со значительными выходами по току. [25]
Самоокисление а-феландрена ведет к образованию перекисных соединений, подобных получаемым при окислении а-терпинена, но перекись а-феландрена гораздо менее устойчива и при 110 - 120 и давлении 3 мм взрывается. [26]
Поглощение кислорода связано с образованием перекисных соединений. Максимальное количество поглощенного кислорода составляет 0 23 - 0 28 моля кислорода на моль структурной единицы, после чего наблюдается скачкообразный переход в трехмерный полимер. [27]
Окисление циклогексана, сопровождающееся образованием перекисных соединений, при возможном накоплении и перегреве-которых может происходить их бурное разложение со взрывом. [28]
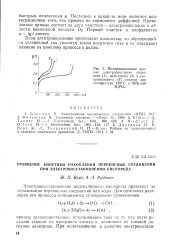 |
Поляризационные кривые электроокисления этилового ( /, метилового ( 2 и изо-пропилового ( 3 спиртов при температуре 120 С в 85 % - ной Н3Р04. [29] |
Электровосстановление молекулярного кислорода протекает до образования перекисных соединений или воды. [30]
Страницы: 1 2 3 4