Образование - фаза - переменный состав
Cтраница 2
Металлы и сплавы выделены в особый раздел М, потому что около 80 % всех элементов составляют металлы, а последние в чистом виде или в виде сплавов являются основными конструкционными материалами в современной технике и промышленности. Ограниченная и неограниченная растворимость металлов, образование фаз постоянного и переменного состава ( интерметаллидов), фаз замещения и внедрения, совокупность физико-химических свойств сплавов определяются многими факторами: индивидуальной природой металлов, размерами их атомов, строением их электронной оболочки и положением элементов в периодической системе. [16]
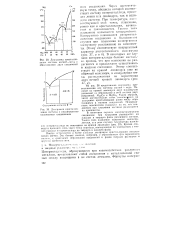 |
Диаграмма кристаллизации системы магнии-медь с образованием двух соединений.| Диаграмма кристаллизации системы с инконгруэнтно плавящимся соединением. [17] |
Иногда встречаются и более сложные диаграммы кристаллизации металлических систем. Это бывает связано, например, с образованием фаз переменного состава, с сочетанием образования соединений и рядов твердых растворов и другими особенноегямп. [18]
В системах Ап - Bv - CVI, кроме рассмотренных уже типов соединений, возможно взаимодействие и по принципу образования твердых растворов замещения. Это обстоятельство ( структурная аналогия) позволяет предположить возможность образования фаз переменного состава в системах А В - AnCVI. Исследования последних систем развиваются. [19]
Из диаграммы а следует, что при очень низких давлениях кислорода ( - lgPO215 2 при 1300 К) в равновесии находятся Се2О3 и Fe. Дальнейшее повышение давления кислорода ( - lgPo2A 14 6) приводит к образованию фазы переменного состава со структурой флюорита СеСЬ - ж, которая вплоть до - IgPo 10 2 остается индифферентной по отношению к железу. Лишь при более высоком давлении образуется ортоферрит CeFeO3, который для составов с реСО 5 сосуществует с флюоритной фазой, а для составов с ре0 5 - сначала с металлическим Fe, а по мере повышения давления - с вюститом и, наконец, с магнетитом. Окислительный распад ортоферрита происходит при парциальных давлениях кислорода, которым отвечает область существования магнетита в бинарной системе Fe - О. Диаграмма рис. 1.17 позволяет оценить составы сосуществующих фаз. [20]
 |
Рентгенографические данные образцов двуокиси марганца. [21] |
В табл. 10 приведены величины удельного сопротивления разных двуокисей марганца. Эта величина оказывает существенное влияние на скорость движения электронов при твердофазном восстановлении двуокиси марганца с образованием фаз переменного состава. Чем меньше удельное сопротивление, тем легче осуществляется этот процесс. С другой стороны, диффузия ионов водорода в твердой фазе облегчается с уменьшением степени кристалличности. Наиболее высокие характеристики имеют элементы с электролитической двуокисью марганца ЭДМ-2 и ГАП, которые имеют наименьшее удельное сопротивление и низкую степень кристалличности. [22]
 |
Дистектические диаграммы состояния с твердыми растворами. [23] |
Методами физико-химического анализа установлено, что в системах элементов главных подгрупп третьей и пятой групп обнаруживаются химические соединения состава A111 Bv ( например, AlSb, GaAs, InSb и др.), являющиеся полупроводниками большого значения. Физико-химический анализ играет большую роль в металловедении, в синтезе интерметаллических и полупроводниковых соединений, в теории образования фаз переменного состава, в галургии и в других специальных областях физической химии. [24]
АШВУ ( например, AlSb, GaAs, InSb и др.), являющиеся полупроводниками большого значения. Физико-химический анализ играет большую роль в металловедении, в синтезе интерметаллических и полупроводниковых соединений, в теории образования фаз переменного состава, в галургии и в других специальных областях физической химии. [25]
Андерсен [259] в 1946 г. в работе Условия равновесия нестехиометрических химических соединений не только весьма убедительно теоретически обосновал необходимость изменения валентного состояния компонентов при образовании фаз переменного состава, но и доказал возможность непрерывного перехода от одного соединения к другому, обладающему кристаллической решеткой даже принципиально другой симметрии. [26]
Из приведенного обзора видно, что до последнего времени не было полной ясности в механизме процесса гидротермического превращения и процессов, сопровождающих закалку продукта, поскольку основные соображения базировались на сопоставлении косвенных данных. В первую очередь необходимо было более глубоко изучить механизм замещения фтор-иона ионом гидроксила с точки зрения возникновения новых фаз, а именно: происходит ли здесь превращение фторапатита в гидроксилапатит или процесс протекает через образование фазы переменного состава - гидроксилфторапатита. Решение этого вопроса представляет не только теоретический интерес, но имеет и. [27]
Показано, что процесс взаимодействия водяного пара с фторапатитом в присутствии кремнезема является многостадийным. Первой стадией является изоморфное замещение иона фтора гидроксильным ионом. Это замещение происходит с образованием фазы переменного состава, содержащей гидроксилфторапатит. Образование этой фазы доказано путем определения теплот образования фторапатита, гидроксилапатита и гидроксилфторапати-та и подтверждено рентгеноструктурным и микроскопическим анализами. [28]
Было установлено, что оптимальная температура, обеспечивающая полное отделение фтора, 1450 - 1500 С. Концентрации водяных паров, образующихся при сжигании жидкого или газообразного топлива, равной 14 %, достаточно для достижения высокой степени обесфторивания. Присутствие кремнезема ускоряет реакцию обесфторивания, кремнезем также необходим для связывания Са и образования силикофосфатной фазы переменного состава, отличающейся высокой растворимостью в 2 % - ной лимонной кислоте, растворе цитрата аммония и хорошо усваиваемой растениями и животными. [29]
Марганец и хром, согласно кривым упругости диссоциации, дают с азотом либо твердый раствор, либо твердый раствор определенного соединения в избытке металла. Для титана данные упругости диссоциации довольно не надежны, но все же скорее говорят за образование фазы переменного состава. [30]
Страницы: 1 2 3