Образование - хинон
Cтраница 1
Образование хинонов из ароматических соединений облегчается в тех случаях, когда в получающихся соединениях Двойные связи в а, р-положении к карбонильной группе соединены с ал-кильными или ароматическими группами. Например, 2-метилна-фталин легко окисляется в 2-метилнафтохйнон - 1 4 благодаря наличию в последнем метильной и ароматической групп в а, 5-поло-жениях к карбонильной группе. [1]
Образование хинонов из ароматических соединений облегчается в тех случаях, когда в получающихся соединениях двойные связи в положениях 1 2 к карбонильной группе соединены с алкильными или ароматическими группами. Например, 2-метил-нафталин легко окисляется в 2-метил - 1 4-нафтохинон благодаря наличию в последнем метильной и ароматической групп в положениях 1 2 к карбонильной группе. [2]
Образование хинонов из - ароматических соединений облегчается в тех случаях, когда в получающихся соединениях двойные связи в а, р-положении к карбонильной группе соединены с ал-кильными или ароматическими группами. Например, 2-метилна-фталин легко окисляется в 2-метилнафтохинон - 1 4 благодаря наличию в последнем метильной и ароматической групп в а, р-поло-жениях к карбонильной группе. [3]
Образование хинонов из ароматических соединений облегчается в тех случаях, когда в получающихся соединениях двойные связи в а, ( - положении к карбонильной группе соединены с ал-кильными или ароматическими группами. Например, 2-метилна-фталин легко окисляется в 2-метилнафтохинон - 1 4 благодаря наличию в последнем метильной и ароматической групп в а, ( i-поло-жениях к карбонильной группе. [4]
Образование хинонов из углеводородов всегда происходит легче, если двойные связи в а, ( 3-положении к карбонильной группе стабилизированы алкильными и в особенности арильными группами. Так, например, бензол лишь в особо специфических условиях с трудом удается прямо окислить в хинон ( с помощью перекиси серебра), антрацен же довольно гладко окисляется в антрахинон, фенантрен-в фенантренхкнон; нафталин по окисляемости занимает промежуточное положение. Окисление может быть осуществлено хромовой кислотой, перекисью водорода или кислородом воздуха в присутствии пятиокиси ванадия. [5]
Образование хинонов из ароматических соединений облегчается в тех случаях, когда в получающихся соединениях двойные связи в а, ( - положении к карбонильной группе соединены с ал-кильными или ароматическими группами. Например, 2-метилна-фталин легко окисляется в 2-метилнафтохинон - 1 4 благодаря наличию в последнем метильной и ароматической групп в а, Р - ПОЛО-жениях к карбонильной группе. [6]
Образование хинонов из ароматических соединений облегчается в тех случаях, когда в получающихся соединениях двойные связи в а, р-положении к карбонильной группе соединены с ал-кильными или ароматическими группами. Например, 2-метилна-фталин легко окисляется в 2-метилнафтохинон - 1 4 благодаря наличию в последнем метильной и ароматической групп в а, Р - ПОЛО-жениях к карбонильной группе. [7]
Образование хинона не является следствием прямого окисления гидрохинона кислородом. Реакция проходит через стадию образования пере-кисных производных мономера, обладающих высокими окислительными свойствами. [8]
Образование хинонов из ароматических соединений облегчается в тех случаях, когда в получающихся соединениях двойные связи в а, р-положении к карбонильной группе соединены с алкильными или ароматическими группами. Например, 2-метилнафталин легко окисляется в 2-метилнафтохинон - 1 4 благодаря наличию в последнем метильной и ароматической групп в, р-положениях к карбонильной группе. [9]
Образование хинонов из углеводородов облегчается в том случае, если двойные связи в а, ( - положении к карбонильной группе стабилизованы алкильными или особенно арильными группами. Напротив, антрацен довольно легко превращается в антрахинон, а фенантрен в фенантренхи-нон, в то время как нафталин занимает среднее положение. [10]
Образование хинонов при торможении окисления фенолами иногда ( при введении большого количества фенола) приводит к замедленному развитию реакции после израсходования всего введенного фенола. [11]
Образование хинонов из углеводородов всегда происходит легче, если двойные связи в - положении к карбонильной группе стабилизированы алкильными и в особенности арильны-ми группами. Так, например, бензол лишь в особых условиях с трудом удается прямо окислить в хинон ( пероксидом серебра), антрацен же, напротив, довольно гладко переходит в антра-хинон, а фенантрен - в фенантренхинон; нафталин в этом ряду занимает промежуточное положение ( ср. Окисление может быть осуществлено хромовой кислотой, пероксидом водорода или кислородом воздуха в присутствии пентаоксида ванадия. [12]
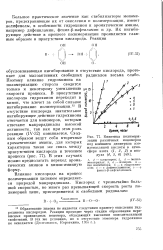 |
Кинетика полимеризации различных мономеров под влиянием динитрила азо-изомасляной кислоты в атмосфере азота ( 1, 2, 3 и воздуха ( 4, 5, 6. [13] |
Образование хинона не является следствием прямого окисления гидрохинона кислородом. Реакция проходит через стадию образования пере-кисных производных мономера, обладающих высокими окислительными свойствами. [14]
Образование хинона легко обнаружить по появлению коричневой окраски. [15]
Страницы: 1 2 3 4