Образование - хлоргидрат
Cтраница 2
Следует также иметь в виду, что давление в системе может колебаться, если создаются перебои эвакуации хлора вследствие нарушения стока кислоты из сушильных башен при прекращении ее циркуляции, а также в результате образования хлоргидратов при понижении температуры влажного газа в холодильниках или трубопроводах ниже 10 С. Во избежание этого внешние хлоропро-воды иногда снабжают паровыми спутниками или намеренно понижают концентрацию газа, например, путем организованного подсоса воздуха через сушильные башни. [16]
В реактор / ( рис. 4.1) подаются хлорбензол, дипропиламин и газообразный хлористый водород в количестве 1 1 моль на 1 моль дипропиламина. Реакция образования хлоргидрата проходит с выделением теплоты, за счет которой температура раствора повышается до 80 С. Непрореагировавший хлористый водород поступает в барботажный абсорбер, где поглощается водой с образованием 2 % НС1, которая идет на нейтрализацию. Затем в реактор 1 подается фосген в количестве 1 25 моль на 1 моль дипропиламина. Реакция фосгенирования протекает при температуре 115 - 130 С. Непрореагировавший фосген и выделяющийся при реакции хлористый водород с примесью паров дипропиламина и хлорбензола поступают через обратный холодильник 2 в абсорбционную наса-дочную колонну 3, орошаемую 5 - 20 % раствором NaOH. Фосген и хлористый водород взаимодействуют с едким натром с образованием хлористого натрия. За счет теплоты реакции температура в колонне повышается до 35 - 45 С. [17]
Легкость окисления адамсита установили также Сергеев и Горский1, показавшие, что адамсит в растворе тетралина ( в присутствии влаги) окисляется уже на холоду кислородом воздуха в фенарсазиновую кислоту. При нагревании адамсита в тетралинозом растворе при 100 - 120 имеет место образование хлоргидрата фенарсазиновой кислоты ( бесцветные игольчатые кристаллы темп. [18]
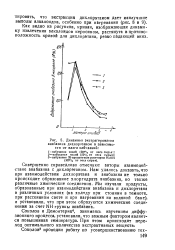 |
Динамика экстрагирования анабазина дихлорэтаном в зависимости от влаги набуханий. [19] |
Совершенно справедливо отмечают авторы взаимодействие анабазина с дихлорэтаном. Нам удалось доказать, что при взаимодействии дихлорэтана и анабазина не только происходит образование хлоргидрата анабазина, но также различные химические соединения. Мы изучали продукты, образованные при взаимодействии анабазина и дихлорэтана в различных условиях ( на холоду при стоянии в темноте, при рассеянном свете и при нагревании на водяной бане), и установили, что при этом образуются химические соединения за счет NH группы анабазина. [20]
Сжижение хлора по двухступенчатой схеме обусловливает необходимость тщательной осушки от влаги исходного хлоргаза для защиты от коррозии оборудования и трубопроводов, на второй стадии сжижения при минус 60 С. При недостаточно тщательной осушке исходного хлор-газа на второй стадии сжижения возможны конденсация воды, образование твердого хлоргидрата, льда и соляной кислоты вследствие гидролиза хлора. Даже при хорошей осушке хлора количества твердого хлоргидрата или льда могут составить 10 - 20 г на 1 т жидкого хлора. Это приводит к образованию легкой мути, немедленно исчезающей при нагревании жидкого хлора, так как растворимость хлоргидрата и воды очень быстро возрастают. [21]
До сих пор для пептидов использовались исключительно метиловые эфиры. Этерифицируют обычно или перед ацилирова-нием, в абсолютном метаноле с сухим газообразным НС1, что приводит к образованию хлоргидратов метиловых эфиров соответствующих пептидов, или же после ацилирования - с помощью диазометана. Если соединение содержит дополнительные карбоксильные группы, как, например, глутаминовая или аспараги-новая кислоты, то они хорошо метилируются в тех же условиях. [22]
Для аммиака и алифатических аминов такой затраты энергии не требуется, так как эти соединения не имеют двойных связей, с которыми электронная пара атома азота могла бы вступить в сопряжение. Действительно, в случае первичных алифатических аминов тепловой эффект солеобразования составляет 13 ккал, в то время как при образовании хлоргидрата анилина тепловой эффект равен всего 7 4 ккал. Разность - 5 6 ккал, очевидно, и соответствует той затрате энергии, которая требуется для нарушения в анилине сопряжения ароматического ядра со свободной электронной парой азота. [23]
Для аммиака и алифатических аминов такой затраты энергии не требуется, так как эти соединения не имеют двойных связей, с которыми электронная пара атома азота могла бы вступить в сопряжение. Действительно, в случае первичных алифатических аминов тепловой эффект солеобразования составляет 13 ккал, в то время как при образовании хлоргидрата анилина тепловой эффект равен всего 7 4 ккал. Разность 5 6 ккал, очевидно, и соответствует той затрате энергии, которая требуется для нарушения в анилине сопряжения ароматического ядра со свободной электронной парой азота. [24]
Для процесса применяют моноэтаноламин с 15 % - ным содержанием воды. Последняя немедленно разлагает тионилхлорид на SOz и НС1 с выделением большого количества тепла; реакционную массу охлаждают до - 6, при этих условиях идет образование хлоргидрата этаноламина. Далее при добавлении всего количества тионилхлорида и поднятия температуры до 30 и затем выдержки при 70 идет хлорирование, с заменой гидрок-сила на хлор. При этом получают густую сиропообразную массу, из которой выпадает осадок хлоргидрата р-хлорэтиламина. [25]
Таким образом, имеющиеся в литературе сведения позволяют считать поиск фунгицидов в ряду производных 1 3-тиазина перспективным. Показано, что во всех случаях, кроме N-трет-бутилтиомочеви - цы, происходит присоединение по СС-связи через атом серы и внутримолекулярное ацилирование вторичного атома азота с образованием хлоргидратов 4-оксо - 3-алкил ( арил) - 2-имино-пергидро - 1 3-тиазинов, которые при нагревании до температуры плавления или кипячении в ледяной уксусной кислоте перегруппировываются в хлоргидраты 4-оксо - 2-алкил ( арил) - имино-пергидро - 1 3-тиазинов. Осторожной нейтрализацией хлоргидратов выделены соответствующие основания. [26]
Хлор ограниченно растворяется в воде с образованием так называемой хлорной воды. Максимальная растворимость хлора в воде при 0 С и атмосферном давлении, равная 1 46 г в 100 г раствора. Последнее объясняется образованием хлоргидрата ( С1О2 - 8Н2О), растворимость которого меньше, чем самого хлора. При температуре ( - 0 24 С) насыщенный раствор хлора замерзает с выделением кристаллов хлоргидрата и льда. Теплота растворения хлора в воде равна 20 8 кДж / моль. [27]
Склонность флавантрона и его производных к образованию стабильных гидратов подтверждает предположение о присоединении одного моля гидрата окиси натрия. Переход желтого цвета в зеленый под действием сильного солнечного света на хлопок, окрашенный флавантроном, вероятно, вызывается образованием лейкокислоты IX. Ввиду основности невосстановленного пиридинового кольца в соединении IX возможно образование хлоргидрата. Восстановление флавантрона цинковой пылью и едким натром при 70 - 80 в атмосфере водорода приводит к образованию темного зеленовато-синего а-тетрагидрофлавантрона ( X), наряду с небольшим количеством а-гексагидропроизводного. Под действием фосфора и иодистоводородной кислоты при 140 - 190 флавантрон превращается в р-тетрагидрофлавантрон ( XI) - зеленое вещество, переходящее при обработке щелочами в енольную модификацию красного цвета. [28]
Интересным методом превращения алкилгалогенидов в первичные амины является также реакция их с гексаметилентетрамином: 1 моль последнего и немногим более 1 моля йодистого натрия в 8 - 10-кратном количестве ( от веса гексаметилентетрамина) 95-проц. При стоянии от нескольких минут до недель, в зависимости от длины цепи алкилгалогенида, образуется продукт присоединения. Последний разлагают путем насыщения смеси газообразным хлористым водородом с образованием хлоргидрата, и амин выделяют путем перегонки хлоргидрата с избытком щелочи. [29]
Дезактивация аминогрупп может наступить в результате вышеупомянутой реакции с ацетилхлоридом, либо за счет образования соли ионного типа с хлористым водородом. С одной стороны утверждают [38], что они столь же реакционно-способны, что и свободные амины; по сведениям других авторов [55], образование хлоргидратов приводит к снижению скорости поликонденсации; при этом меняются оптимальные условия проведения реакции. Практика показывает, что процессы низкотемпературной растворной поликонденсации носят более длительный характер, чем это должно быть судя по константам ацилирования. Не исключено, что участие в реакции хлоргидратов диаминов является одной из причин снижения суммарной скорости процесса. [30]
Страницы: 1 2 3