Образование - циангидрин
Cтраница 1
Образование циангидринов зависит от строения атомов или групп, находящихся у карбонильного углерода. Как уже упоминалось выше, влияние заместителей на состояние карбонильной двойной связи и пространственные эффекты может быть столь значительным, что вообще не будет происходить присоединения цианистого водорода. Так, например, бензальдегид или ацетофенон еще образуют циангидрины, однако чисто ароматический кетон, бензофенон, к этому уже не способен ( о мезомерном эффекте фенильных групп см. стр. Для кетонов С9 - Си образование циангидринов очень затруднено, циклический кетон С10, по-видимому, практически вообще не образует циангидрина. Возможно, что здесь проявляется пространственный эффект, так как именно у этих циклов особенно велико питцеровское напряжение ( см. стр. [1]
Образование циангидринов кетонов менее выгодно, и в результате 1 4-присоединение приводит к р-цианкетону. [2]
С кетонами образование циангидринов происходит труднее, а в некоторых случаях между кетоном и синильной кислотой не наблюдается никакой реакции. [3]
В ходе образования циангидринов получается смесь нитрилов D-глюконовой и D-манно-новой кислот. [4]
Скорость реакции образования циангидринов и константа равновесия этой реакции возрастают по мере увеличения частичного положительного заряда на карбонильном углероде. Все заместители с - / - и - М - эффектами действуют ускоряюще. [5]
Важной особенностью реакции образования циангидринов является необходимость основного катализа. В отсутствие основания реакция либо не происходит, либо протекает очень медленно. [6]
В этой реакции совмещается образование циангидрина и обычная аль-дольная реакция. На первой стадии анион цианида присоединяется к молекуле бензальдегида. [7]
В случае цианистого водорода образование циангидрина обычно происходит быстрее, чем 1 4-присоединение, и если положение равновесия выгодно ( как для большинства альдегидов), то наблюдается только 1 2-присоединение. [8]
При получении гормона тестостерона образование циангидрина использовалось для защиты одной из кетогрупп Д4 - андростен-3 17-диона I, чтобы сделать возможным дальнейшее ее избирательное превращение. [9]
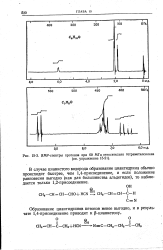 |
ЯМР-спектры протонов при 60 МГц относительно тетраметилсилана. [10] |
В случае цианистого водорода образование циангидрина обычно происходит быстрее, чем 1 4-присоединение, и если положение равновесия выгодно ( как для большинства альдегидов), то наблюдается только 1 2-присоединение. [11]
Ясно, что скорость образования циангидрина падает в тем большей степени, чем сильнее карбонильная группа экранирована алкильными группами. Все же диизопропилкетон реагирует еще почти так же быстро, как ацетон, и лишь ди-трег-бу-тилкетон, в котором карбонильная группа сильно экранирована, практически уже не может образовать циангидрина. [12]
Какая из них приводит к образованию циангидрина. [13]
Присоединение цианида к альдегиду с образованием циангидрина делает возможным потерю протона с образованием резонансно-стабилизованного аниона LXIX. Обратное присоединение протона, но уже к атому углерода, соседнему с карбоксильной группой, с последующей кетонизацией дает ацилцианид - активный ацилирующий агент, который быстро реагирует с водой или спиртом, давая предельную кислоту или эфир. [14]
Реакционная способность карбонильных соединений при образовании циангидринов тщательно исследована. Большая часть альдегидов реагирует, образуя равновесные смеси с высоким содержанием продуктов реакции, хотя бензальдегид реагирует гораздо медленнее, чем большинство альдегидов алифатического ряда. [15]
Страницы: 1 2 3