Обратимость - электродный процесс
Cтраница 2
В разделах 7.3.3 и 7.3.4 рассматривались отклонения от обратимости электродных процессов, обусловленные замедленностью переноса заряда. Однако в некоторых типах систем могут преобладать кинетические эффекты, вызванные сопряженными химическими реакциями или адсорбцией, и часто отклонения от обратимости можно объяснить этими эффектами, а не замедленным переносом заряда. Работа [11] содержит прекрасный пример некоторых влияний сопряженных химических реакций на электродные процессы. В этой же работе подробно рассматриваются адсорбционные эффекты. [16]
Оценим возможности хронопотенциометрического метода, исходя из критерия обратимости электродных процессов. [17]
Хотя логарифмические графики и другие диагностические критерии установления обратимости электродного процесса чрезвычайно полезны и широко используются в аналитической работе, все же наиболее однозначным методом исследования обратимости является изучение предполагаемого продукта электродного процесса, как это было отмечено в разд. [18]
Пространственное расположение пиков катодного и анодного токов позволяет судить об обратимости электродного процесса. [19]
Осциллографическая кривая потенциал-время может быть использована прежде всего для исследования обратимости электродных процессов. В случае обратимости процесса кривая имеет строго симметричную форму. [20]
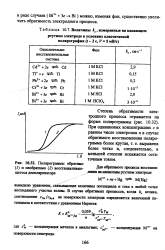 |
Величины ks, измеренные на капающем.| Полярограммы обратимо ( 1 и необратимо ( 2 восстанавливающегося деполяризатора. [21] |
Зе - Bi) можно, изменяя фон, существенно увеличить обратимость электродного процесса. [22]
 |
Прибор АУ-4М. [23] |
Напряжение, прилагаемое к двум индикаторным электродам, зависит от степени обратимости электродных процессов, в которых участвует реагент и определяемое вещество. Чем больше обратимость системы, тем меньшее напряжение требуется налагать на электроды. [24]
Если число электронов известно, это же уравнение можно использовать для оценки обратимости электродного процесса, сравнивая экспериментальную величину котангенса угла наклона с теоретической. [25]
Уравнения полярографических волн, рассмотренные в предыдущих главах, были выведены в предположении обратимости электродного процесса. Это означает, что равновесие между окисленной и восстановленной формами деполяризатора и электродом устанавливается так быстро, что потенциал электрода подчиняется уравнению Нернста, а величина тока определяется только скоростью диффузии деполяризатора к электроду и от электрода. Однако лишь относительно небольшое число процессов на ртутном капельном электроде протекают обратимо. [26]
Очевидно, соответствие между Ер и Ег / 2ие может быть использовано для определения обратимости электродного процесса. [27]
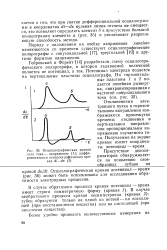 |
Осциллографическая кривая сила тока - напряжение ( 7. дифференциальная осциллографическая кривая di-de, ( 2. [28] |
Осциллографическая кривая потенциал - время ( рис. 36) может быть использована для исследования обратимости электродных процессов. [29]
 |
Поведение платинового и стеклянного ( ЭО-021 электродов в системе Се4 3 ( 0 5 М H2SO4. [30] |
Страницы: 1 2 3 4 5