Обсуждение - механизм
Cтраница 3
 |
Ингибирование метилметакрила - пикрилгидразила в бензоле получетом цепного распада перекиси бензоила в но уравнение. растворе этилацетата. [31] |
При обсуждении механизма химических реакций, протекающих при распаде перекиси бензоила в том или ином растворителе, необходимо принимать во внимание цепной распад перекиси. [32]
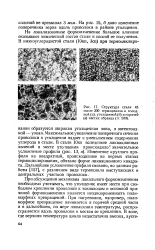 |
Структура стали 45 после 200 термоциклов в холодной ( а, утолщенной ( б и горячей ( в частях образца ( X 500. [33] |
При обсуждении механизма локального формоизменения необходимо учитывать, что утолщение имеет место при свободном креплении проволоки к токовводам и основной причиной формоизменения является неодновременность полиморфных превращений. При нагревании, например, полиморфное превращение начинается в горячей средней части и в дальнейшем, по мере повышения температуры, распространяется вдоль проволоки к местам ее крепления. [34]
При обсуждении нейронных механизмов научения следует учитывать две возможности: непрерывную реверберацию импульсов и изменение связей между элементами. При этом электрические сигналы могут запустить биохимический синтез, который затем определяет структурные изменения. Электрические сигналы могут также направить синтез специфических макромолекул, структура которых кодирует информацию на входе. [35]
При обсуждении механизма химических реакций, протекающих при распаде перекиси бензоила в том или ином растворителе, необходимо принимать во внимание цепной распад перекиси. [36]
При обсуждении механизма превращения ацетилена принимается во внимание, что в тлеющем разряде при низких давлениях, характеризующемся наличием высоких электронных и низких молекулярных температур, имеются благоприятные условия для образования значительных количеств свободных радикалов и атомов. [37]
При обсуждении механизма перегруппировок бромидов, в частности того воззрения, что эти реакции протекают через отщепление и обратное присоединение бромистого водорода, но в другом порядке, следует иметь в виду высокую температуру. Действительно, при этом имели место под действием высокой температуры реакции отщепления бромистого водорода. [38]
При обсуждении механизма каталитического выделения водорода на ртутном электроде в растворах комплексов металлов с органическими и неорганическими лигандами определенную роль приписывают частицам с низким состоянием окисления центрального атома. В монографии [74] рассмотрены основные идеи, касающиеся трактовки механизма выделения водорода и особой роли комплексов и их устойчивости в этом процессе. Поэтому здесь следует лишь отметить, что гипотеза о роли интермедиатов в каталитическом выделении водорода на ртутном электроде в растворах комплексов металлов, о которых упоминалось в разделе 1.3.3, в последнее время снова привлекла интерес исследователей. Способностью стабилизировать необычно низкие состояния окисления переходных металлов, по-видимому, обладают многие лиганды, содержащие электронодонорные атомы ( азота, серы и фосфора) с вакантными разрыхляющими я - орбиталями. [39]
При обсуждении механизма действия защитных веществ механизм инактивации радикалов играет доминирующую роль. [40]
При обсуждении механизма окислительной конверсии метанола в формальдегид авторы работы [48] предполагают, что из находящихся на поверхности серебра ионов кислорода О -, О2 -, 02, наименее прочно связан с катализатором ион 02 -, благоприятствующий образованию диоксида углерода, более прочно связан с катализатором ион О -, ответственный за мягкое окисление метанола в формальдегид, и, наконец, наиболее прочно связанный с катализатором ион О2 -, способствует образованию формальдегида по реакции дегидридования метанола. Таким образом, наличие наиболее прочно связанных с серебром ионов О-и О2 - повышает селективность процесса. Результаты показали, что отрицательный заряд увеличивает выход формальдегида, а положительный - уменьшает. Наложение заряда меняет соотношение между кислородными ионами и, следовательно, изменяет вклад отдельных реакций. О -, как наиболее прочно связанных с поверхностью катализатора, и селективность процесса повышается. [41]
При обсуждении ферстеровского механизма переноса энергии от донора к акцептору, который рассматривался в разд. [42]
При обсуждении механизма действия ингибиторов кислотной коррозии металлов чаще всего используют результаты, полученные с помощью наиболее распространенной модельной реакции катодного выделения водорода. Это вполне оправдано, так как чаще всего именно-эта реакция определяет скорость коррозии металлов в кислотах. Сопоставление величин г и Y полученных при изучении влияния ингибиторов на реакцию анодного растворения металлов, с величиной 6, как правило, экспериментально осуществить трудно. Это объясняется тем, что при потенциалах анодного растворения металлов строение границы металл - раствор значительно усложняется. Измеряемые величины емкости имеют высокие значения и связаны, в основном, с протеканием фарадеевского анодного процесса, адсорбцией анионов раствора, в частности, ионов гидроксида. [43]
Уже из обсуждения механизма электрополимеризации ясног что, в отличие от гальванического осаждения металлов, только стартовая реакция следует закону Фарадея. Дальнейшие реакции уже не носят электрохимического характера и представляют собой процесс полимеризации винилсодержащих соединений. По скорости электрополимеризация является реакцией первого порядка относительно концентрации мономера в растворе. [44]
Для простоты обсуждения механизмов целесообразно введение системы их классификации. В работе Варфоломеева, Наки, Ярополова, Побочина ( 1981) для описания механизмов сложных химических и ферментативных реакций предложена и использована система, основанная на записи последовательности различных стадий процесса. Важно то обстоятельство, что в стационарном состоянии в уравнение скорости реакции входят лишь параметры лимитирующих стадий и стадий, предшествующих скорость-определяющей. Быстрые, нелимитирующие стадии процесса, следующие за наиболее медленной, не оказывают влияния на скорость реакции и не проявляются в кинетике процесса. [45]
Страницы: 1 2 3 4