Окисел - металл
Cтраница 1
Окисел металла содержит 47 06 % кислорода, а соединение того же металла с бромом - 89 88 % брома. [1]
Окисел металла содержит 28 57 % кислорода, а соединение того же металла с фтором 48 72 % фтора. [2]
Окисел металла содержит 78 7 % металла и 21 3 % кислорода. Вычислите атомный вес металла, если его удельная теплоемкость равна 0 05 кал / г-град. [3]
Окисел металла содержит 17 02 % кислорода, а соединение того же металла с йодом - 76 51 % йода. [4]
Если окисел металла в условиях опыта обращается в жидкое состояние и сдувается с поверхности металла, он перестает служить препятствием к быстрому окислению металла. Примером этого может служить железо. Этот факт горения металла, имеющий большое практическое значение, был открыт вскоре после открытия кислорода. Мы опишем этот опыт в варианте, наглядно разъясняющем химическую суть явления. [5]
Если окисел металла в условиях опыта обращается в жидкое состояние и сдувается с поверхности металла, он перестает служить препятствием к быстрому окислению металла. Примером этого может служить железо. Этот факт горения металла, имеющий большое практическое значение, был открыт вскоре после открытия кислорода. Мы опишем этот опыт словами Лавуазье в варианте, наглядно разъясняющем химическую суть явления. [6]
Если окисел металла легко химически взаимодействует с носителем, может образоваться соединение, которое значительно устойчивее к восстановлению, чем сам окисел. Эта картина наблюдается при попытках диспергировать Мо03 или WO3 на таких носителях, как окись алюминия или двуокись кремния с высокой поверхностью. Молибдат алюминия также не образуется [8], и аналогичная ситуация, по-видимому, будет наблюдаться и для вольфрама. Весьма вероятно, что при указанных концентрациях молибден и вольфрам находятся в виде поверхностных окислов, имеющих толщину порядка монослоя и расположенных на поверхности окиси алюминия. Естественно, что в обоих случаях восстановление до металла водородом при температурах вплоть до 820 К не происходит, хотя в случае молибдена [8, 10] ( но не вольфрама [9]) наблюдается некоторое восстановление до состояния ниже шестивалентного. [7]
Эквивалент окисла металла равен его формульному молекулярному весу, деленному на число атомов металла в его формульной молекуле и на валентность этого металла. [8]
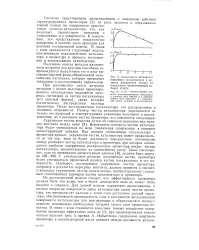 |
Зависимость активности никелевого катализатора в реакции разложения метана от содержания промотирующей добавки ( СаО. [9] |
Получение окисла металла разложением нитратов или другими способами сопровождается выделением его в виде высокодисперсной фазы, образованной мельчайшими частицами, которые проявляют тенденцию к последующему укрупнению. [10]
Активное взаимодействие окисла металла с радикалами ускорителя еще не означает, что данный окисел хороший активатор вулканизации. [11]
Для получения окисла металла из руды, в которой металл содержится в виде окисла, гидроокиси, сульфида, силиката или соли другого металла с кислотой, образованной данным металлом, применяют различные методы. [12]
Таким образом, окисел металла входит в силикатную сгр уктуру не как свободный окисел, а определенным образом взаимодействует с ним, деполимеризуя силикатный каркас. [13]
Осадок прокаливают; образовавшийся окисел металла ( в данном случае закись-окись Со3О4) взвешивают. [14]
Осадок прокаливают; образовавшийся окисел металла ( в данном случае закись-окись СозО взвешивают. [15]
Страницы: 1 2 3 4