Окисел - металл
Cтраница 4
При добавлении в реакционную смесь окисла легковосстана-влнваемого металла он также восстанавливается алюминием и даст соответствующий сплав с титаном, цирконием или другим металлом. Вследствие этого активность титана снн / кается, и равновесие смещается в сторону восстановления его окисла. [46]
Разложение соли в вакууме позволяет получать окисел металла с большой поверхностью. Если реакция экзотермическая, то чем ниже температура разложения соли, тем активнее катализатор. Однако во время каталитического процесса часто не удается сохранить высокую активность контакта. [47]
При разложении нагреванием 0 2318 г окисла металла получено 0 2158 г металла. [48]
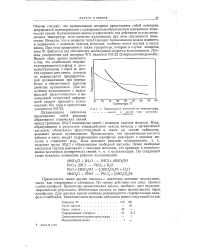 |
Зависимость вязкости от температуры. [49] |
Вода, образующаяся в результате взаимодействия окисла металла с органической кислотой, обязательно присутствующей в смеси на основе хайпалона, вызывает начало вулканизации. Предполагают, что органическая кислота ( обычно в смесь вводят гидрированную канифоль) реагирует с окислом металла и отщепляет воду. [50]
При восстановлении водородом 7 2 г окисла металла образуется 1 8 г воды. [51]
При этом в результате реакции получается смесь окисла металла и черного угольного порошка. Точно так же смесь порошка магния с твердым снегом, состоящим из СО2, может быть подожжена и сгорает, образуя смесь белой MgO и черных частиц угля. [52]
Так, продуктами реакции трифторида брома и окисла металла ( например, Nb205) является кислород, бром и фторид металла. Механизм этой реакции замещения неизвестен, однако роль BrF3 нельзя сводить только как к простому источнику F -, так как в этом случае фтор был бы столь же эффективен, чего на самом деле нет. Трифторид брома представляет собой исключительно эффективный растворитель для многих неорганических фторидов, так как он образует комплексы [25, 26], в которых фтор является как донором, так и акцептором. [53]
Страницы: 1 2 3 4