Окисление - спирт
Cтраница 1
Окисление спиртов реактивом Коллинза проводят в хлористом метилене обычно при 25, используя шестикратный молярный избыток реагента. Реакция завершается в течение 5 - 15 мин. Реагент, в частности, рекомендуется для окисления первичных спиртов до альдегидов. [1]
Окисление спиртов осуществляют с помощью двух основных [ риемов - дегидрирования и действия окислителей. [2]
Окисление спиртов может быть осуществлено с помощью различных соединений металлов. Наиболее широко используют соединения хрома ( VI), перманганат калия и диоксид марганца; применяют также соединения меди, платины, серебра, рутения и ванадия. [3]
 |
Электролизер для влектроокисления спиртов.| Конструкция электродного блока. [4] |
Окисление спиртов проводят одновременно в двух электролизерах, соединенных последовательно. По заданию преподавателя изучают эффективность окисления двух различных спиртов либо одного и того же спирта при различных температурах или плотностях тока. [5]
Окисление спиртов в кислых, практически безводных растворах может также давать ацетали или кетали в качестве промежуточных или побочных продуктов. Метод, по-видимому, не имеет практической ценности для получения ацеталей и редко применяется для получения кеталей. [6]
Окисление спиртов осуществляют с помощью двух основных риемов - дегидрирования и действия окислителей. [7]
 |
Важнейшие реакции спиртов. [8] |
Окисление спиртов обычно проводят сильными окислителями - хромовой смесью или смесью перманганата калия с серной кислотой. [9]
Окисление спиртов до альдегидов или кетонов и альдегидов до кислот является обычной химической ( а также микробиологической) реакцией, которая лишь в редких случаях не может быть осуществлена. Поэтому в настоящей главе микробиологические методы обсуждаются постольку, поскольку с их помощью в ряде случаев может быть достигнута большая избирательность реакции, чем та, которую обеспечивают традиционные химические способы. [10]
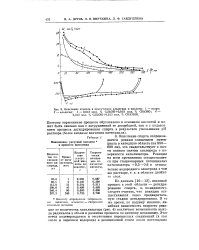 |
Окисление этанола в присутствии альдегида и кислоты. 1 - спирт. 2 - альдегид. 3 - 0 013 мол. % С2Н5ОН 0 013 мол. % СН3СНО. 4 - 0 013 мол. % С2Н5ОН 0 013 мол. % СН3СООН. [11] |
Окисление спирта сопровождается резким смещением потенциала в катодную область ( на 550 - 600 мв), что свидетельствует о почти полном снятии кислорода с поверхности катализатора. [12]
Окисление спиртов хромовой кислотой протекает по ионному механизму. [13]
Окисление спиртов в лабораторных условиях чаще всего осуществляется с помощью хромовой кислоты ( Н2Сг04), которую обычно по мере надобности получают из трехокиси хрома ( Сг03) или из бихромата натрия ( Na2Cr207) в сочетании с серной кислотой. В качестве наиболее удобного растворителя для таких реакций обычно используется уксусная кислота. [14]
Окисление спиртов по Оппенауэру в теоретическом отношении представляет собой пример окислительного процесса с переносом гидрид-иона от восстановителя к окислителю в одну стадию, в то время как в ранее описанных процессах окисление спиртов осуществляется в несколько последовательных стадий и сопровождается последовательным переносом одного или нескольких электронов. [15]
Страницы: 1 2 3 4