Окисление - ферроцен
Cтраница 1
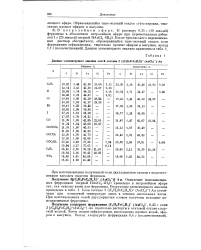 |
Данные элементарного анализа солей состава 3 [ ( СбШРеСбШХ ( АиСЦ - ] - Аи. [1] |
Окисление монозамещен-ных ферроценов твердой НАиСЛ4 - 4Н2О проведено в петролейном эфире так, как описано выше для ферроцена. Соли состава 3 [ ( C5H6FeC6H4X) ( АиС14) - ] - Аи устойчивы при комнатной температуре лишь в течение нескольких часов. При восстановлении солей двухлористым оловом получены исходные мо-нозамещенные ферроцены. [2]
В работе [254] изучено окисление ферроцена и би-ферроценила ( Fc-Fc) на платиновом электроде в органических растворителях - ацетонитриле и хлористом метилене. [3]
Так, ЕН волны окисления ферроцена равен Ек волны восстановления катиона феррициния. ЕХ, что также говорит в пользу обратимости этой системы. В связи с исследованием явлений адсорбции ферроцена, наблюдающихся при восстановлении катиона феррициния в водных растворах [2-5], доказательство обратимости этой системы особенно важно, поскольку в случае полной обратимости и при преимущественной адсорбции продукта, согласно теории Брдички, на полярограммах растворов соли феррициния должны возникать адсорбционные предволны. Для более строгой проверки обратимости системы ферроцен - катион феррициний мы применили переменнотоковую полярографию. [4]
Тот факт, что при окислении ферроцена циклопентадие-нильные кольца, как в случае циклопентадиенилида пиридиния, не затрагиваются, свидетельствует, видимо, о достаточно прочной связи атома железа с этими кольцами. [5]
Методом переменнотоковой полярографии показано, что окисление ферроцена на капельном ртутном катоде в 60 - 96 % - ном этаноле протекает обратимо. На это указывает наличие пиков на кривых активной и реактивной составляющих переменного тока, совпадение потенциалов пиков, близость ширины полупиков к 88 мв и равенство высот пиков. Область адсорбции ферроцена с анодной стороны ограничена потенциалом окисления ферроцена, а с катодной - слабо выраженным пиком десорбции. [6]
Рассмотрим теперь влияние состава растворителя на предельные диффузионные токи восстановления катиона феррициния и окисления ферроцена и на величины потенциалов полуволн. [7]
Исследование системы ферроцен - катион феррициний методом перемен-нотоковой полярографии мы начинаем с изучения окисления ферроцена, поскольку этот процесс, который приходится изучать в растворах с высоким содержанием этанола, значительно меньше осложнен адсорбционными явлениями. [8]
Формальные электродные потенциалы были определены полярографически для восстановления ионов таллия и рубидия и для окисления ферроцена. [9]
В работе [47] с помощью переменнотоковой вольтамперометрии ( кривые dE / dt - Е) было установлено, что окисление ферроцена и его производных на ртутном и платиновом анодах действи-тельно протекает обратимо. Потенциал, соответствующий точке перегиба на кривой окисления ферроцена, зависит от природы заместителя. [10]
Значение ф0 22 0 300 В ( потенциал ф0 22 соответствует фтг / 4 на кривой окисления), найденное из кривой восстановления продукта окисления ферроцена, приблизительно совпадает с фт / 4 0 307В, что указывает на обратимость процесса. [11]
Холл и Рассел [46] исследовали упомянутые корреляционные соотношения повторно, используя как собственные данные ( см. табл. 13.4), так и результаты других авторов. Потенциалы окисления ферроценов с заместителями амидного типа, связанными с кольцом через атом азота, необычно малы. Считают, что это обусловлено прямым взаимодействием заместителя с атомом железа в окисленной молекуле. [12]
Следует заметить, что во всех случаях, когда реагенты не содержат групп СОСН3, CN и С1, в реакционную среду добавляется алюмин иевая пыль, как это делает в своей реакции Е. О. Фишер, в отношении 1: 1 к соединению ферроцена. Это мешает нежелательному окислению ферроцена в феррициний-катион, что легко происходит под действием хлористого алюминия. Что касается феррициний-катиона, он в этой реакции не обменивает лиганда. Группы СОСН3 и CN восстанавливаются под действием А1 / А1С13, однако именно в случае этих групп применение алюминиевой пыли и не нужно, так как заместители - акцепторы электронов препятствуют окислению ферроцена. [13]
В отличие от предыдущих томов с ферроценовой тематикой, в которых в основном уделялось внимание проблемам электрофилыюго замещения в циклопептадиенильном лиганде, в этом томе превалируют работы по исследованию свойств ферроцена и его различных производных, например, таких, как ферроцепилкарбинолы и генетически связанные с ними ферроценилкарбониевые ионы. Уделяется большое внимание проблемам окисления ферроценов в феррициний-катионы. В этот том вошли работы А. Н. Несмеянова по синтезу мостиковых производных ферроцена, интерес к которым был обусловлен идеей, которую А. Несмеянов высказал еще 25 лет назад на одном из коллоквиумов по металлооргапической химии на Химическом факультете МГУ. Речь шла о возможности синтеза на основе мостиковых производных ферроцена соединений типа атом в клетке, в которых свободный атом металла находился бы в углеводородной клетке, причем связь атома металла с этой клеткой была бы обусловлена только геометрическими причинами. [14]
При переходе от чисто водного раствора к этаноловому величины ЕЙ становятся более положительными приблизительно на 200 же. Волны восстановления катиона феррициния и окисления ферроцена в этаноле очень близки к потенциалу начала анодного растворения ртути. При любом составе растворителя величины Е восстановления катиона феррициния и окисления ферроцена практически совпадают ( рис. 6), что удовлетворяет критериям обратимости электродного процесса. [15]
Страницы: 1 2 3