Окисление - хинолин
Cтраница 1
Окисление хинолина и его производных перманганатом калия в зависимости от имеющихся заместителей и от экспериментальных условий приводит к образованию пирндинкарбоновых кислот, производных антраниловой кислоты, производных изатина или бензоксазолонов. [1]
Окисление хинолина азотной кислотой осуществляется в две стадии: 1) окисление до хинолиновой кислоты; 2) декарбоксили-ронание. Предложен и одностадийный процесс окисления хинолина до никотиновой кислоты смесью концентрированных серной и азотной кислот. Катализатором служит молнбдат аммония. Этот способ не принят для внедрения в промышленность из-за отсутствия материалов, устойчивых к действию такой смеси кислот, а также из-за других его недостатков. [2]
Окисление хинолина щелочным перманганатом дает хино-линовую ( 2 3-пиридиндикарбоновую) кислоту. [3]
Изучено окисление хинолина с целью синтеза никотиновой кислоты [128, 129], которая образуется в результате декарбок-силирования при обработке электролита, содержащего хиноли-новую кислоту, в свою очередь полученную электроокислением хинолина. [4]
Хотя окисление хинолина и алкилхинолинов перманганатом калия или пероксидом водорода приводит обычно к расщеплению цикла, как описано ниже, однако есть возможность и окислить алкильную боковую цепь до карбоксильной группы, не разрушая цикла. [5]
При окислении хинолина перманганатом получают хинолиновую кислоту, которая может быть декарбоксилирована в никотиновую кислоту ( ср. [6]
При окислении хинолина было разрушено кольцо, не содержащее азота, и таким образом совершен переход к а Р - пиридин-дикарбоновой кислоте. [7]
При окислении хинолина перманганатом в щелочной среде образуется 2 3-пиридиндикарбоновая ( хинолиновая) кислота. [8]
При окислении хинолина было разрушено кольцо, не содержащее азота, и таким образом совершен переход к а, 3-пиридин-дикарбоновой кислоте. [9]
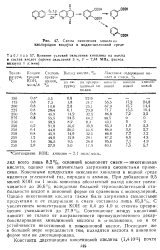 |
Схема окисления хинолина кислородом воздуха в водно-щелочной среде.| Влияние условии окисления хинолина на выход к состав кислот ( время окисления 3 ч, Р - 7 84 МПа, расход воздуха 1 л / мин. [10] |
Конечными продуктами окисления хинолина в водной среде являются углекислый газ, пиридин и аммиак. При добавлении 0 5 молей КОН на 1 моль хинолина абсолютный выход кислот увеличивается до 36 6 % вследствие большей термоокислительной стабильности кислот в анионной форме по сравнению с. Соотношение между кислотами, зависит не только от направленности преимущественного декар-боксилирования хинолиновой кислоты в u - положении, но и от устойчивости никотиновой и пиколиновой кислот. Последнее же в большей мере определяется тем, находится кислота в анионной форме или не диссоциирована. [11]
Обычные методы окисления хинолина требуют применения дорогих и дефицитных окислителей, например перманга-ната калия [2-4], перекиси водорода [26, 29], или применения концентрированных кислот ( серной, азотной или их смесей) при высокой температуре и высоком давлении [5-11], что создает трудности в аппаратурном и технологическом оформлении процесса. Каталитические методы [27] и применение озона для окисления хинолина [28], хотя и перспективны, но требуют специальной и довольно сложной аппаратуры. [12]
Недостатком метода окисления хинолина серной кислотой является: высокая температура, сложное аппаратурное оформление процесса, обильное выделение сернистого газа и токсичность катализатора - селена. [13]
Представляет определенный интерес окисление хинолина кислородом в водно-щелочной среде. Процесс позволяет получить никотиновую кислоту высокой степени чистоты ( 98 5 %) в одну стадию. [14]
В основу реакции окисления хинолина положен метод Вудварда [116], заключающийся в окислении хинолина серной кислотой при температуре 300 С в присутствии катализатора - металлического селена. [15]
Страницы: 1 2 3 4