Окисление - алкилбензол
Cтраница 3
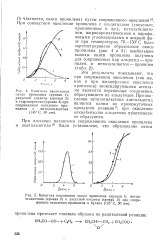
Несколько позднее ( в 1912 г.) Чамичан и Зильбер2 изучали окисление алкилбензолов кислородом в присутствии влаги на прямом солнечном свету. Процесс обычно проводился в течение многих месяцев при нормальных температуре и давлении. [31]
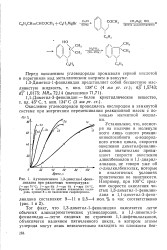 |
Аутоокисление 1 3-диметил - 1-фени-линдана при различных температурах. [32] |
Установлено, что, несмотря на наличие в молекуле всего лишь одного реакци-онноспособного а-водород-ного атома цикла, скорости окисления диметилфенилин-данов значительно превышают скорости окисления алкилбензолов и 1 1-диарил-алканов, не говоря уже об о-диалкилбензолах, которые в аналогичных условиях практически не окисляются. [33]
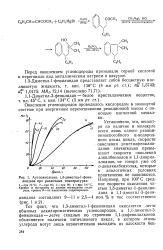 |
Аутоокисление 1 3-диметил - 1-фени-линдана при различных температурах. [34] |
Установлено, что, несмот ря на наличие в молекуле всего лишь одного реакци-онноспособного сс-водород-ного атома цикла, скорости окисления диметилфенилин-данов значительно превышают скорости окисления алкилбензолов и 1 1-диарил-алканов, не говоря уже об о-диалкилбензолах, которые в аналогичных условиях практически не окисляются. [35]
Ядра ароматических углеводородов окисляются труднее нафтеновых циклов и алифатических углеводородных цепей. Так, при окислении алкилбензолов в первую очередь окисляются боковые цепи. [36]
Показано [155], что при окислении ж-ксилола высокой активностью по сравнению с активностью солей двухвалентного кобальта обладают комплексные соединения катализатора состава Со2 ( А) 3 ( ОН) 2, где А-анион. Образование активных комплексных соединений катализаторов окисления алкилбензолов с а-бромсукцииимидом [156], с карбонильными галогенными и другими соединениями [154, 157] показывают, что изменение активности катализатора связано, по-видимому, с изменением окислительно-восстановительного потенциала катиона металла под влиянием лиганд и с его координационной насыщенностью. Тем не менее в ряде случаев отмечается снижение каталитической активности катиона металла под влиянием лиганд. Так, при окислении о-ксилола в среде уксусной кислоты активность кобальта снижается, что, по мнению исследователей [47], связано с возможностью образования неактивного хелатного комплекса с фталевой кислотой. [37]
Эти результаты показывают, что при сопряженном окислении ( так же, как и при жидкофазном окислении пропилена) эпоксидирующими агентами являются перекисные соединения, образующиеся из альдегидов. При окислении метилэтилкетона ацетальдегид является одним из промежуточных продуктов реакции9; при окислении алкилбензолов альдегиды практически не образуются. [39]
Высокая промотирующая способность брома и его соединений, сочетающаяся со специфическими свойствами повышать селективность реакции по отношению к целевым продуктам, позволила в одну стадию с высоким выходом получить фтале-вые кислоты. В СССР и за рубежом этот способ разработан и освоен в промышленном производстве. В табл. 2.1 приведены катализаторы, растворители и температурные условия реакции окисления алкилбензолов, нашедших применение в промышленной практике. [40]
Алкилнафталины так же, как и алкилбензолы, по нашим данным [148], в тех мягких условиях, при которых изучалось окисление алканов и алкенов ( при 50 С в течение 100 час), окисляются плохо. Поэтому для накопления продуктов их окисления потребовалось максимальное из всех проведенных нами опытов увеличение времени до 130 час и повышение температуры до ШО С. По количеству присоединенного кислорода, принимая во внимание максимальную температуру опыта, склонность алкил-нафталинов к окислению меньше склонности к окислению алкилбензолов и тем более ялканов и алкенов. На основании экспериментальных данных можно сделать общий для алкилбензолов и алкилнафталинов вывод о том, что увеличение их молекулярного веса за счет величины жирного радикала приводит к ухудшению их склонности к окислению. [41]
При получении устойчивых гидропероксидов окислением алкил-бензолов образуются побочные продукты ( за счет частичного разложения гидропероксидов), являющиеся большей частью ингибиторами процесса, причем количество этих примесей зависит от глубины превращения алкилбензола. На образование побочных продуктов существенное влияние оказывает температура: чем она выше, тем меньше выход гидропероксида ( в расчете на прореагировавший углеводород) и больше побочных продуктов. В то же время при низкой температуре недостаточна скорость окисления. При окислении алкилбензолов в соответствующие гидропероксиды начальная температура окисления поддерживается на уровне 120 - 130 С. По мере накопления гидропероксидов в реакционной смеси температуру снижают, и конечная температура обычно бывает около 105 - 108 С. [42]
Страницы: 1 2 3