Окисление - двуокись - сера
Cтраница 3
СО, окисление двуокиси серы и др.) - Катализаторы полидисперсной структуры могут быть в несколько раз активнее монодисперсных. [31]
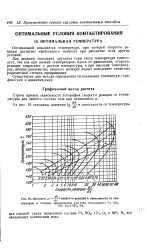 |
Значения х - - L скорости реакции в зависимости от температуры и степени превращения для газа, содержащего 7 SCh 11 % О2 и 82 % Nj. [32] |
Для реакции окисления двуокиси серы такая температура существует, так как при низких температурах, вдали от равновесия, скорость реакции возрастает с ростом температуры, а при высоких температурах, вблизи-равновесия, скорость реакции падает вследствие снижения равновесной степени превращения. [33]
Поскольку реакция окисления двуокиси серы связана с изменением числа молекул, численное значение константы равновесия зависит от того, в каких единицах выражается состав газовой смеси. [34]
В случае окисления двуокиси серы образование комплекса из двух молекул SO2, способного взаимодействовать с молекулой кислорода, мало вероятно, так как для образования такого-комплекса должно Сыть преодолено значительное электростатическое отталкивание полярных молекул двуокиси серы. [35]
Ускорение реакции окисления двуокиси серы под влиянием окислов азота является одним из первых получивших известность примеров каталитического действия. [36]
Поскольку реакция окисления двуокиси серы связана с изменением числа молекул, численное значение константы равновесия зависит от того, в каких единицах выражается состав газовой смеси. [37]
Ускорение реакции окисления двуокиси серы под влиянием окислов азота является одним из первых получивших известность примеров каталитического действия. [38]
Вследствие экзотермичности окисления двуокиси серы и большой начальной скорости реакции при высоком содержании двуокиси серы в газовой смеси, как это имело место в опытах Книтча, неизбежен разогрев газовой смеси в начальной зоне катализатора на несколько десятков градусов. [39]
При процессе окисления двуокиси серы в серную кислоту катализатором является двуокись азота. Двуокись азота ассимилирует, вещество среды с образованием новых молекул, склонных к внутримолекулярным реакциям и к выделению образовавшихся веществ во внешнюю среду, с регенерацией катализатора для нового процесса. [40]
Кинетика процесса окисления двуокиси серы во взвешенном слое катализатора в значительной степени определяется гидродинамическими факторами. Кроме интенсивного радиального и осевого перемешивания возможен проскок газа в виде пузырей. Учесть все факторы очень трудно. Однако опытно-промышленные и промышленные испытания показывают, что в реакторах большого диаметра достигаются условия полного перемешивания. [41]
Скорость реакции окисления двуокиси серы зависит от температуры, активности катализатора и концентрации реагирующих веществ. Возрастанию скорости реакции, но затрата энергии на сжатие газа экономически не оправдывается повышением выхода. [42]
Третьим механизмом окисления двуокиси серы служит окисление в жидко-капельной фазе облаков и туманов. Реакции могут носить каталитический характер, при этом скорость возрастает на 1 - 2 порядка. Однако скорость выведения двуокиси серы из атмосферы определяется не только химическими реакциями, но и вероятностью попадания молекулы в жидкофазную среду. Эта вероятность, в свою очередь, зависит от множества факторов: климатических условий региона, времени года, высоты выброса двуокиси серы над поверхностью земли, значения рН облачных и дождевых капель. [43]
В производственных условиях окисление двуокиси серы обычно осуществляют, пропуская поток газа через слой катализатора; состоящий из пористых зерен с развитой внутренней поверхностью. В этом случае надо учитывать два типа процессов переноса: 1) обмен между газовым потоком и внешней поверхностью зерен катализатора и 2) перенос вещества и тепла внутри зерен катализатора. [44]
В производственных условиях окисление двуокиси серы обычно осуществляют, пропуская поток газа через слой катализатора, состоящий из пористых зерен с развитой внутренней поверхностью. В этом случае надо учитывать два типа процессов переноса: 1) обмен между газовым потоком и внешней поверхностью зерен катализатора и 2) перенос вещества и тепла внутри зерен катализатора. [45]
Страницы: 1 2 3 4