Количественное окисление
Cтраница 1
Количественное окисление до Аш ( VI) наблюдается при концентрации 242Ст ие более 0 16 мг / мл. [1]
Количественное окисление арсенита возможно только при связывании выделяющихся в реакции ионов гидроксония. С другой стороны, значение рН системы не должно быть слишком большим, так как в противном случае установится равновесие 12 ОН - 1 - ЮН, при котором невозможно определить конечную точку титрования по образованию соединения иода с крахмалом. [2]
Количественное окисление фосфитов происходит в течение 20 мин. [3]
Количественное окисление тиосульфата перманганатом в сульфат про-исходит только в щелочном растворе, в кислом же растворе тиосульфат окисляется до сульфата и тетратионата. [4]
Количественное окисление тиосульфата перманганатом - в сульфат про-исходит только в щелочном растворе, в кислом же растворе тиосульфат окисляется до сульфата и тетратионата. [5]
Количественное окисление полимеров, в особенности элементоорганических, или продуктов их термической обработки, содержащих конденсированные углеродные - циклы, затруднено. Окисление этих веществ даже при высокотемпературном сожжении сопровождается образованием коксоподобных остатков и расплавов оксидов гетероэлементов, в которых заключены частицы несгоревшего вещества. Результаты по азоту получаются заниженными. Такой способ позволяет правильно анализировать полимеры, содержащие карборановые ядра, полиариленбензимидазолы и другие подобные вещества и продукты их термолиза. [6]
Количественное окисление органических соединений, содержащих таллий, до минерализации последнего, обычно производят дымящей азотной кислотой при нагревании [1], причем соединения жирного ряда разрушаются довольно легко, тогда как для разрушения ароматических соединений требуется довольно продолжительное нагревание. Затем, после восстановления серной кислотой, таллий определяется весовым путем в виде иодида или хромата. [7]
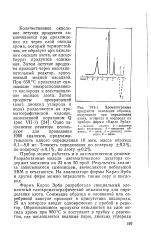 |
Хроматограмма продуктов окисления образца, полученная при определении азота, углерода и водорода на приборе фирмы Карло Эрба. [8] |
Количественное окисление летучих продуктов заканчивается при прохождении их через слой оксида хрома, который термоустойчив, не образует яри окислении оксидов азота, не адсорбирует продуктов сожжения. Затем летучие продукты проходят через восстановительный реактор, заполненный медной насадкой. При 650 С происходит связывание неизрасходованного кислорода и восстановление оксидов азота. [9]
Такое количественное окисление наиболее ценно для выяснения структуры углеводов. [10]
После количественного окисления образца до муравьиной кислоты избыток окислителя обратно оттитровывают сульфатом железа ( И) с N-фенил-антраниловой кислотой в качестве индикатора. [11]
Изящным методом количественного окисления или восстановления является метод с использованием электронообменных смол. При их применении посторонние ионы, за исключением ионов гидроксония, не попадают в раствор. Поскольку окислительно-восстановительный потенциал этих обменников зависит также от рН и структуры смолы, его можно варьировать в широких пределах. [12]
Чтобы достигнуть количественного окисления арсенита до арсената, связывают ионы водорода бикарбонатом. [13]
А при количественном окислении даст maximum 1.47 г янтарной кислоты и 0.6 г щавелевой; вещество формы Б maximum может дать 0.73 г янтарной кислоты. Отсюда ясно, что, получив янтарной кислоты больше 0.73 г, я разрешаю задачу в пользу формы А. [14]
При этом достигается полное количественное окисление углерода до двуокиси углерода, измеряемой при помощи газовой бюретки. [15]
Страницы: 1 2 3 4