Каталитическое окисление - двуокись - сера
Cтраница 3
Для решения вопроса о природе соединения, обусловливающего каталитическую активность промышленных ванадиевых катализаторов, необходимо выяснить, какие ванадиевые соединения устойчивы в условиях каталитического окисления двуокиси серы. [31]
На основании этих данных можно заключить, что из соединений пятиокиси ванадия с окислами щелочных металлов только поливанадаты и сульфованадаты щелочных металлов устойчивы в условиях каталитического окисления двуокиси серы. [32]
Из окисей, исследованных Гернет и Хитун [106] ( окиси кальция, магния, стронция, цинка, алюминия, висмута, марганца, никеля, кобальта и меди), не все оказались промоторами при добавлении к катализатору Сг203 - 8пОг, употребляемому при каталитическом окислении двуокиси серы. Окись бария и окись железа ясно активировали катализатор. Для окисей элементов с четным атомным числом наблюдается меньшее отрицательное влияние, чем для элементов с нечетными атомными числами. [33]
Первое предложение получать серную кислоту контактным способом путем окисления двуокиси серы кислородом воздуха в присутствии платиновых катализаторов было сделано Филлипсом в 1831 г. Это предложение долгое время не использовалось, и только в 70 - х годах прошлого столетия появились первые установки, на которых осуществлялось каталитическое окисление двуокиси серы кислородом на глати-новом катализаторе. [34]
Первое предложение получать серную кислоту контактным способом путем окисления двуокиси серы кислородом воздуха в присутствии платиновых катализаторов было сделано Филлипсом в 1831 г. Это предложение долгое время не использовалось, и только в 70 - х годах прошлого столетия появились первые установки, на которых осуществлялось каталитическое окисление двуокиси серы кислородом на платиновом катализаторе. [35]
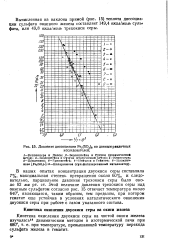 |
Давление диссоциации Fe2 ( SO4 a по данным различных. [36] |
В наших опытах концентрация двуокиси серы составляла 7 %, максимальная степень превращения около 60 %, и следовательно, парциальное давление трехокиси серы было около 82 мм рт. ст. Этой величине давления трехокиси серы над окисным сульфатом согласно рис. 15 отвечает температура около 640, являющаяся, таким образом, тем пределом, при котором гематит еще устойчив в условиях каталитического окисления двуокиси серы при работе с газом указанного состава. [37]
Образование серной кислоты в современных промышленных нитрозных установках ( так называемый бгшенный способ производства серной кислоты) также представляет собой сложный гетерогенный процесс, существенной стадией которого является растворение двуокиси серы и окислов азота в серной кислоте. Гомогенное каталитическое окисление двуокиси серы не имеет места в нитрозном процессе. [38]
Гетерогенное каталитическое окисление двуокиси серы лежит в основе одного из технологических методов получения серной кислоты. [39]
Образование серной кислоты в современных промышленных нитрозных устанонках ( так нгзываемый бгшенный способ производства серной кислоты) также представляет собой сложный гетерогенный процесс, существенной стадией которого является растворение двуокиси серы и окислов азота в серной кислоте. Гомогенное каталитическое окисление двуокиси серы не имеет места в нитрозном процессе. [40]
Это позволяет предположить, что причиной снижения каталитической активности ванадиевых катализаторов в результате прогрева при высоких температурах ( выше 600) является превращение активного компонента катализатора в ванадил-ванадаты. В условиях каталитического окисления двуокиси серы ванадил-ванадаты представляют собой наиболее устойчивую твердую фазу, содержащую ванадий. Переход кислых ванадатов в соответствующие ванадил-ванадаты может поэтому осуществляться с конечной скоростью при температурах ниже температуры плавления данной смеси. [41]
Страницы: 1 2 3