Глубокое окисление - органическое вещество
Cтраница 1
 |
Коэффициенты диффузии в пористых оксидных катализаторах [ 129. [1] |
Глубокое окисление органических веществ является экзотермической реакцией, в результате чего наблюдается разогревание катализатора и реакционной смеси. [2]
 |
Концентрация летучих примесей в атмосфере орбитальной станции Скайлэб [ 26, с. 185 - 196 ]. [3] |
Глубокое окисление органических веществ может служить не только для очистки атмосферы от вредных примесей, но и использоваться как источник тепла. [4]
Кинетика глубокого окисления органических веществ зависит от многих факторов, в том числе от свойств окисляемых веществ и катализаторов, а также условий проведения реакции. [5]
Реакции глубокого окисления органических веществ катализируются переходными металлами и их окислами. Наиболее активны металлы платиновой группы и окислы железа, меди, хрома и других металлов. Отличительной особенностью процессов термокаталитической очистки является отсутствие системности в свойствах катализаторов и окисляемых веществ, поэтому можно рассматривать лишь некоторые их характерные тенденции. [6]
Реакции глубокого окисления органических веществ практически необратимы, что позволяет при наличии подходящих катализаторов полностью превратить токсичные органические вещества в безвредные продукты - диоксид углерода и воду. [7]
Реакции глубокого окисления органических веществ катализируются переходными металлами и их окислами. Наиболее активны металлы платиновой группы и окислы железа, меди, хрома и других металлов. Отличительной особенностью процессов термокаталитической очистки является отсутствие системности в свойствах катализаторов и окисляемых веществ, поэтому можно рассматривать лишь некоторые их характерные тенденции. [8]
Реакции гетерогенного каталитического глубокого окисления органических веществ имеют специфику, которая сказывается на кинетике. [9]
 |
Зависимость выхода метилакролеина ( МА ( 1 и СО2 ( 2 от концентрации О2 в импульсе. [10] |
Кинетические уравнения реакций глубокого окисления органических веществ ( как и других каталитических реакций), выведенные без учета воздействия реакционной среды на катализатор, не отражают действительного механизма каталитической реакции. Даже хорошее соответствие рассчитанных по этим уравнениям и экспериментально определенных скоростей реакций не может рассматриваться как подтверждение справедливости представлений о механизме рассматриваемой реакции, использованных при выводе этих уравнений, пока не будет установлена идентичность кинетики реакции для стационарного и нестационарного состояния катализатора. [11]
Поскольку в процессе глубокого окисления органических веществ вследствие экзотермичности реакции в слое катализатора могут развиваться высокие температуры, необходимо чтобы катализатор был термостойким. Обычно под термостойкостью катализатора подразумевают его способность сохранять свою активность в процессе работы при высоких температурах. К сожалению, многие катализаторы, обладающие большой начальной активностью, теряют ее в результате работы при высоких температурах, вследствие спекания и уменьшения поверхности. [12]
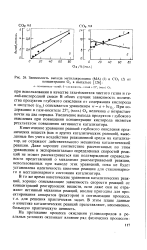 |
Зависимость выхода метилакролеина ( МА ( 1 и СО2 ( 2 от концентрации О2 в импульсе. [13] |
Кинетические уравнения реакций глубокого окисления органических веществ ( как и других каталитических реакций), выведенные без учета воздействия реакционной среды на катализатор, не отражают действительного механизма каталитической реакции. Даже хорошее соответствие рассчитанных по этим уравнениям и экспериментально определенных скоростей реакций не может рассматриваться как подтверждение справедливости представлений о механизме рассматриваемой реакции, использованных при выводе этих уравнений, пока не будет установлена идентичность кинетики реакции для стационарного и нестационарного состояния катализатора. [14]
Современная трактовка механизма глубокого окисления органических веществ в растворах кислородных соединений хлора основана на теории, в соответствии с которой эти вещества реагируют с кислородом, предварительно переведенным в активное состояние в результате разложения соединений хлора. В связи с этим представляется целесообразным использование в технологии электрохимической деструкции органических загрязняющих веществ катализаторов разложения соединений хлора на хлорид-ионы и атомарный кислород, обладающий еще более высокой реакционной способностью по сравнению с активным хлором. [15]
Страницы: 1 2 3 4