Кривое окисление
Cтраница 1
Кривые окисления показывают ( рис. 7.13), что под действием озона сульфонафтеновые кислоты окисляются несколько легче, чем нафтеновые. Расход озона на окисление при рН 12 5 составляет 4 61 мг на 1 мг нафтеновых кислот и 3 97 мг на 1 мг сульфонафтеновых кислот. [1]
Кривые окисления ВТ-1Д при 1000е в газовых смесях кислорода с азотом представлены на фиг. [2]
Кривые окисления стали 1Х18Н9Т в перегретом паре при 600 и на воздухе при 1100 представлены на фиг. Окисление стали 1Х18Н9Т в указанных средах протекает по логарифмическому закону. [3]
Все кривые окисления идут очень кучно и имеют тенденции к стабилизации процесса через 1000 ч после начала испытаний. [4]
Все кривые окисления водорода на различных металлах начинаются в пределах одной и той же области потенциалов, но затем можно наблюдать значительные различия в интенсивности окисления водорода, потому что каталитические активности разных металлов не одинаковы. Кроме того, активность того же самого металла меняется в зависимости от способа изготовления электрода. [5]
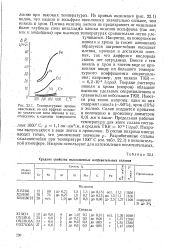 |
Средние свойства высокоомных нагревательных сплавов.| Температурные кривые окисления. но оси ординат отложено увеличение веса образца в час, отнесенное к единице поверхности. [6] |
Из кривых окисления ( рис. 22.1) видно, что железо и вольфрам окисляются значительно сильнее, чем никель и хром. Пленка окислов железа не предохраняет от окисления более глубокие слои металлаУа пленка окислов вольфрама ( так же, как и молибдена) при высоких температурах сравнительно легко улетучивается. Вместе с тем никель и хром в чистом виде не применяют ввиду их большого температурного коэффициента сопротивления; например, для никеля TKR 6 2 - КГ3 1 / град. Твердые растворы никеля и хрома ( нихром) обладают высоким удельным сопротивлением и сравнительно небольшим TKR. Имеется ряд типов нихрома: один из них содержит никель ( - 60 %), хром ( 15 %) и железо. Сплав поддается прокатке и волочению в проволоку диаметром 0 01 мм и выше. Нихромы выпускаются в виде ленты и проволоки. [7]
Нерегулярность кривых окисления ( см. рис. 73) для сталей, с содержанием 0 15 - 0 9 % С ( а также 0 65 % Мп и 0 2 % Si), полученных Зибертом [530] а воздухе при температурах от 950 до 1100 С, по сравнению с регулярной кривой для железа Армко явно обусловлена обезуглероживанием, как это предполагает и сам автор. Даже состав окисных слоев меняется: содержание железа в окалине на углеродоодержащих образцах бывает гораздо ниже. Правда, это может быть за счет содержания в ней марганца и кремния. [8]
Изучение хода кривых окисления подтверждает, что скорость окисления железа, когда на его поверхности образуется слой, состоящий из фазы Fe3O4, значительно медленнее и резко увеличивается с появлением вюститной фазы FeO. Диффузия кислорода через слой Fe3O4 также затруднена, хотя и относительно в меньшей степени. Последние данные по изучению окисления железа с помощью метода электронной дифракции при пониженных давлениях и различных температурах позволили установить, что температуры перехода фаз меняются в зависимости от давления и толщины пленок. Превращение - у - Р Оз в cc - Fe2O3 сопровождается изменением кубической решетки типа шпинель в ромбоэдрическую решетку корундового типа и протекает при 225 С, в то время как превращение Fe2O3 в Fe3O4 в тонких пленках уже происходит при 225 С, а у толстых пленок - при 450 С. [9]
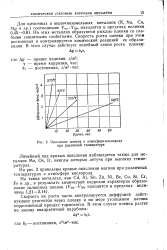 |
Окисление магния в атмосфере кислорода при различной температуре. [10] |
Линейный ход кривых окисления наблюдается также для металлов Mo, Os, Ir, окислы которых летучи при высоких температурах. [11]
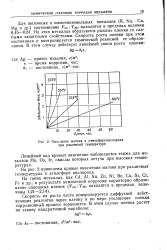 |
Окисление магния в атмосфере кислорода при различной температуре. [12] |
Линейный ход кривых окисления наблюдается также для металлов Mo, Os, IT, окислы которых летучи при высоких температурах. [13]
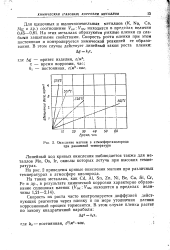 |
Окисление мапния в атмосфере кислорода при различной температуре. [14] |
Линейный ход кривых окисления наблюдается также для металлов Mo, Os, Ir, окислы которых летучи при высоких температурах. [15]
Страницы: 1 2 3 4 5