Элементарный окислитель
Cтраница 2
Магний и бериллий взаимодействуют с элементарными окислителями, причем с галогенами реакция окисления идет энергично только при нагревании. Кислород в обычных условиях окисляет компактный магний и бериллий только с поверхности, так как возникающая при этом оксидная пленка предохраняет металлы от дальнейшего окисления. При высоких температурах магний и бериллий в атмосфере кислорода сгорают, причем особенно интенсивно способен гореть магний. При горении магния происходит интенсивное излучение света, богатого ультрафиолетовыми лучами, что используют в магниевой вспышке при фотографировании. Порошкообразный магний в смеси с твердыми окислителями способен сгорать со взрывом. С серой порошкообразный магний при нагревании реагирует также со взрывом. Магний при высокой температуре способен гореть в азоте с образованием нитрида. [16]
Металлы группы цинка взаимодействуют с элементарными окислителями, особенно активно с галогенами, далее при обычной температуре. В результате взаимодействия с кислородом при обычной температуре на поверхности цинка и кадмия образуется тончайшая оксидная пленка, которая защищает эти металлы ог дальнейшего окисления. При нагревании цинк и кадмий образуют с кислородом оксиды ZnO и CdO. Ртуть довольно легко окисляется кислородом при нагревании до невысокой температуры, однако образующийся оксид HgO, будучи термически непрочным, при высокой температуре легко разлагается. Цинк и кадмий при нагревании образуют с серой сульфиды ZnS и CdS, а ртуть при растирании с серой образует сульфид HgS даже при обычной температуре. С азотом, водородом и углеродом металлы группы цинка в обычных условиях не взаимодействуют. [17]
 |
Свойства оксидов галлия, индия и галлия. [18] |
Металлы группы галлия взаимодействуют с элементарными окислителями. Так же они взаимодействуют и с водородом. [19]
 |
Разности энтальпий образования оксидов некоторых металлов. [20] |
При взаимодействии металлов с такими элементарными окислителями ( как галогены, сера) в основном повторяются те же закономерности, что и при взаимодействии с кислородом: металлы по-прежнему отдают электроны, хотя могут иметь место и некоторые отклонения, что зависит от соотношения электроотрицательностей окислителя и металлов. [21]
Металлы активно вступают во взаимодействие с элементарными окислителями с большой электроотрицательностью ( галогены, кислород, сера и др.) и поэтому при рассмотрении общих свойств металлических элементов необходимо учитывать их химическую активность по отношению к неметаллам, типы их соединений и формы химической связи, так как это определяет не только металлургические процессы при их получении, но и работоспособность металлов в условиях эксплуатации. [22]
В водных растворах различных веществ могут восстанавливаться преимущественно такие элементарные окислители, энергия диссоциации молекул которых сравнительно невелика. [23]
И водных растворах различных веществ могут восстанавливаться преимущественно такие элементарные окислители, энергия диссоциации молекул которых сравнительно невелика. [24]
Щелочные металлы легко вступают в химические реакции со всеми элементарными окислителями: галогенами, кислородом, серой, азотом и даже водородом. [25]
Как сильные восстановители, щелочные металлы взаимодействуют со всеми элементарными окислителями - галогенами, халькогенами, азотом и водородом. [26]
Способность преломлять свет, количественно выражаемая величиной показателя преломления, у различных элементарных веществ различна: у элементарных окислителей, являющихся диэлектриками, и у благородных газов она невелика. У элементарных металлоидов, являющихся полупроводниками, она значительно повышается, а у элементарных металлов, no - существу, становится бесконечно большой. Металлы непрозрачны: их гладкая поверхность отражает падающие на нее световые лучи ( мелко раздробленный металл их поглощает), поэтому они обладают характерным металлическим блеском, интенсивность которого зависит от доли поглощаемого металлом света: чем она меньше, тем ярче блеск. [27]
Способность преломлять свет, количественно выражаемая показателем преломления, у различных элементарных веществ различна: она невелика у элементарных окислителей, являющихся диэлектриками, а также у благородных газов. У элементарных металлоидов, являющихся полупроводниками, она значительно выше, а у элементарных металлов, по существу, становится бесконечно большой. Металлы непрозрачны, при гладкой поверхности падающие на них световые лучи отражаются ( мелко раздробленный металл их поглощает), поэтому для металлов характерен металлический блеск, интенсивность которого зависит от доли поглощаемого металлом света: чем она меньше, тем ярче блеск. Окраска металлов обусловлена тем, что они поглощают лучи различных длин волн не одинаково. Неметаллические элементарные вещества также кажутся окрашенными, если они поглощают видимый свет, хотя бы в определенной области частоты колебаний. [28]
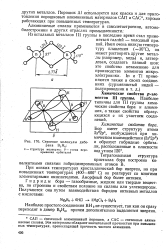 |
Строение молекулы дибо-рана В2Нв. [29] |
При низких температурах кристаллический бор инертен, но при повышенных температурах ( 400 - 600Q С) он реагирует со мшгими элементарными окислителями. Аморфный бор более активен. [30]
Страницы: 1 2 3 4