Окись - ниобий
Cтраница 2
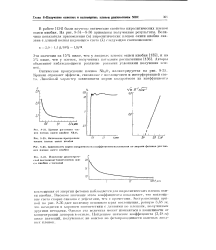
В работе [134] были изучены оптические свойства пиролитических пленок окиси ниобия. На рис. 8 - 84 - 8 - 36 приведены полученные результаты. [17]
Согласно рентгеновским данным, отмечается некоторая растворимость окиси цинка в окиси ниобия и окиси ниобия в окиси цинка, не показанная на диаграмме. В статье Полларда приводятся межплоскостные расстояния и интенсивности для двух указанных ниобатов. [18]
Фаза, выделившаяся по границам зерен, вероятнее всего состоит из окиси ниобия NbO. [19]
Согласно рентгеновским данным, отмечается некоторая растворимость окиси цинка в окиси ниобия и окиси ниобия в окиси цинка, не показанная на диаграмме. В статье Полларда приводятся межплоскостные расстояния и интенсивности для двух указанных ниобатов. [20]
Аналогично можно промотировать и активность окислов металлов V группы, например окиси ванадия или окиси ниобия. [21]
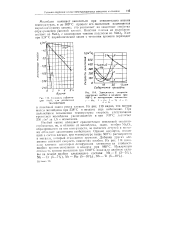 |
Зависимость скорости окисления ниобия в воздухе при С от легирующих элементов. [22] |
Ниобий также обладает сравнительно невысокой окалино-стойкостыо, по, в отличие от молибдена, окись ниобия МЬ2О, образующаяся на его поверхности, не является летучей и поэтому обладает защитными свойствами. Однако кислород, входящий в состав пленки, при температуре выше 500 С растворяется в металле, который становится хрупким. Добавки других элементов снижают скорость окисления ниобия. На рис. 114 показано влияние некоторых легирующих элементов на стойкость ниобия против окисления в воздухе при 980 С. [23]
Ниобий также обладает сравнительно невысокой окалино-стойкостью, но, в отличие от молибдена, окись ниобия Nb2O5, образующаяся на его поверхности, не является летучей и поэтому обладает защитными свойствами. Однако кислород, входящий в состав пленки, при температуре выше 500 С растворяется в металле, который становится хрупким. Добавки других элементов снижают скорость окисления ниобия. На рис. 114 показано влияние некоторых легирующих элементов на стойкость ниобия против окисления в воздухе при 980 С. [24]
Метод основан на том, что тантал осаждается таннином из слабокислых оксалатных растворов легче, чем любой другой окисел вообще и окись ниобия, в частности; первым выделяется танниновый комплекс тантала, вторым - титана и третьим - ниобия. [25]
 |
Соединение вольфрамовых нитей катодов прямого накала с танталовыми токоподводами путем. [26] |
Однако ниобий необходимо обезгаживать в вакууме путем нагревания, продолжающегося примерно 5 мин при температуре 1 i65Q С, и полностью освобождать от окиси ниобия. [27]
Окиси ниобия и тантала сплавляли с персульфатом калия, плав выщелачивали насыщенным раствором оксалата аммония, подкисленного щавелевой кислотой. Окись алюминия предварительно приводили в равновесие с насыщенным раствором оксалата аммония с рН 6 4, вводили в нее ниобий и тантал. Колонку промывали насыщенным раствором оксалата аммония с рН 7 0, причем тантал быстро переходил в фильтрат. [28]
Образование метаниобата или ортониобата редкоземельного элемента отмечается на кривых нагревания большими экзотермическими эффектами при 730 - 740 С. Для механических смесей окисей ниобия и редкоземельных элементов взаимодействие наступает при температурах выше 900 С. [29]
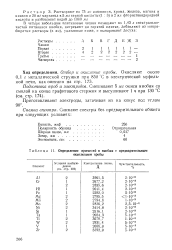 |
Определение примесей в ниобии с предварительным окислением пробы. [30] |
Страницы: 1 2 3 4