Окись - графит
Cтраница 3
В противоположность изложенной точке зрения Вейсс [1110] и Франклин [298] нашли, что структуру окиси графита можно считать аналогичной структуре бисульфата графита. Это означает, что в том случае, когда количество внедренной ( до предела) соли не превышает стехиометрически возможного, не будет наблюдаться перекашивания углеродных сеток, аналогичного перекашиванию при образовании ковалентных связей. Данные, свидетельствующие о наличии перекашивания сеток, кажутся противоречивыми. [31]
Существует предположение, не проверенное, правда, на опыте, что структуры, аналогичные структуре окиси графита, могут образовываться как промежуточные стадии при окислении графита газообразным кислородом, особенно в присутствии молекул воды. По химическим свойствам окись графита при комнатной температуре является вполне устойчивой. Различные структуры окиси графита могут образоваться также в качестве промежуточных продуктов окисления графита паром. Этот вопрос имеет непосредственное отношение к гл. [32]
Рентгенографические исследования [441, 447, 896, 897] показывают, что расстояние между слоями углеродных макромолекул в графите увеличивается при образовании окиси графита. Окись графита в некоторых отношениях отличается от других слоистых соединений. В зависимости от количества введенной воды расстояние между слоями макромолекул меняется от 6 до 11 А. [33]
В этом процессе одна из ОН-групп не поддается ацетилированию, однако при восстановлении с одновременным ацетилированием окиси графита получается меньшее количество иода, чем при прямом восстановлении. Это обстоятельство, возможно, указывает на наличие в окиси графита кетоенольной таутомерии [218, 221], хотя исследование инфракрасного поглощения [372] не выявляет наиболее эффективных связей кислорода с углеродом. [34]
Несмотря на наличие большого числа работ, систематизированных, например, Крофтом [102] и Уббелоде и Льюисом [254], детально структура окиси графита все еще не выяснена. Однако нет сомнения в том, что окись графита имеет слоистую решетку, состоящую из слоев углеродных атомов. Эти слои не являются полностью графитовыми, так как линии о ( 1010) и ( 1120) указывают на то, что расстояние С - С равно 1 44 А, в то время как в графите оно равно 1 41 А. Проекция на плоскость гармошкообразной алифатической гексагональной углеродной сетки с расстоянием С - С, равным 1 53 А, дает для С - С на плоскости решетки величину 1 45 А. Таким образом, величина 1 44 А соответствует решетке, состоящей либо из частично ароматических, либо из гармошко-образных алифатических углеродных слоев. В каждом слое, по-видимому, имеются связанные с ним группы ОН -, кислородные мостики и кето-группы. Межслоевое расстояние в окиси графита, высушенной на воздухе, составляет около 9 А, а в высушенной над пяти-окисью фосфора - 6 3 А. Гидроксильные группы, сохраняющиеся даже после сушки над пятиокисью фосфора, могут быть этерифици-рованы и нейтрализованы. [35]
Рентгенографические и другие исследования сорбции окисью графита широкого класса молекул [161] показывают, что нормальные алифатические спирты могут располагаться между сетками окиси графита или перпендикулярно или вдоль их плоскости. Величина расстояния между сетками, полученная из оценки этого эффекта, оказалась равной примерно 4 8 А. [36]
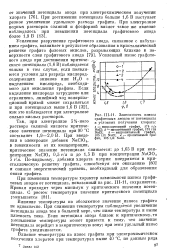 |
Зависимость износа графитовых анодов от потенциала в условиях получения хлората. [37] |
По-видимому, добавки хлората натрия внедряются в кристаллическую решетку графита, способствуя его окислению [80] и снижая энергетический уровень, необходимый для образования окиси графита. [38]
В связи с отсутствием общепринятого термина для обозначения самого высокого продукта окисления графита, еще сохраняющего развитую сеточную структуру, представляется целесообразным использовать общее название окись графита, пока не будут полностью установлены различные формы продукта ( для полноты обзора ср. Включение этого вещества в последовательный ряд кристаллических соединений графита вытекает из следующих соображений. [39]
То обстоятельство, что меллитовая кислота образуется, как правило, без участия окиси графита, когда неграфитизи-рованные углероды подвергаются окисляющему воздействию разбавленных азотной и серной кислот, согласуется с известной точкой зрения, по которой окись графита содержит полигексагональные сетки атомов углерода. [40]
Штауденмайер [978 - 980] и Хамди [385] показали, что в том случае, когда азотная и серная кислоты нагреваются с графитом в присутствии небольшого количества окисляющего агента, например в присутствии хлорноватокислого калия, графит набухает и претерпевает последовательное изменение окраски; в конце концов реакция завершается образованием окиси графита. На первый взгляд кажется странным, что образование бисульфата и других кислых соединений графита происходит аналогичным путем. Однако бисульфат графита образуется лишь в тех случаях, когда концентрированная серная кислота добавляется к графиту в присутствии различных окисляющих агентов. [41]
Это явление можно объяснять тем, что присутствие в растворе указанных окислителей снижает энергетический уровень, нвобходи-мй для образования окнеи графита Участие окислителя но-видн-мому, заключается во внедрении его между слоями кристаллической реяеткн я окислении графита с образованием промежуточных неустойчивых соединений - кислых солей графита, переходящих в результате гидролиза в окись графита. Все эти пронесен сопровождаются набуханием н расслаиванием кристаллической ренеты графита. [42]
Из данных титрования щелочью следует, что концентрация титруемых гидроксильных групп составляет - - 6 - 10 мг-экв / г, в то время как данные опыта эте-рификации с помощью различных реагентов и обмена с ионами кальция приводят к значениям от 0 4 до 7 мг-экв / г. Эти различия можно объяснить присутствием в окиси графита карбоксильных групп с различной кислотностью. При испарении суспензии окиси графита на пластинках пористого стекла были получены мембраны, которые использовались в концентрационных ячейках. Большие катионы легко проникали через мембраны, но ионы натрия и лития вызывали их набухание и деструкцию. [43]
Из данных титрования щелочью следует, что концен - - грация титруемых гидроксильных групп составляет - 6 - 10 мг-экв / г, в то время как данные опыта эте-рификации с помощью различных реагентов и обмена с ионами кальция приводят к значениям от 0 4 до 7 мг-экв / г. Эти различия можно объяснить присутствием в окиси графита карбоксильных групп с различной кислотностью. При испарении суспензии окиси графита на пластинках пористого стекла были получены мембраны, которые использовались в концентрационных ячейках. Большие катионы легко проникали через мембраны, но ионы натрия и лития вызывали их набухание и деструкцию. [44]
Окись графита термически не очень устойчива: если ее быстро нагреть до 200 С, она вспыхивает с выделением СО2, СО, Н2О и мелко раздробленного угля. Окись графита - окислитель и реагирует с различными восстановителями. [45]
Страницы: 1 2 3 4