Биогель
Cтраница 3
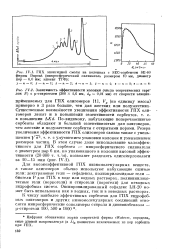
Этот же принцип недавно был использован для разделения 40S и 60S субъединиц рибосом на колонках сефарозы 4В или биогеля А-15 т в солевом растворе неизменной концентрации ( 0 5 М КС1) с помощью изменения температуры. При 4 и указанной концентрации KCI 40S субъединицы очень слабо задерживаются агарозой и выходят четким пиком. Объем элюции лежит примерно посередине между свободным и полным объемами колонки. Затем при той же температуре вымывается пуромицин, использованный для диссоциации рибосом. Для снятия с колонки 60S субъединиц оказывается достаточным повысить температуру элюента до 35 - субъединицы выходят четким пиком [ К. [31]
 |
Характеристика имеющихся в продаже биогелей типа Р. [32] |
В проспектах фирмы указано также, что степень набухания гелей практически не зависит от изменения ионной силы среды; набухание биогеля Р-100 снижается на 2 % при изменении концентрации фосфатного буфера от 0 до 0 4 М [190] ( ср. [33]
Клетки, продуцирующие антитела против конъюгированного антигена азофенил-р-лактозида, можно избирательно отделить от других клеток i [86] на колонке с биогелем Р-6 со связанным гаптеном. [34]
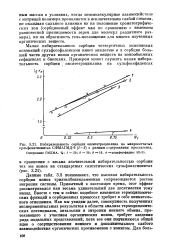 |
Избирательность сорбции окситетрациклина на макросетчатых сульфокатионитах СФМАГМД-6 ( 1 - 3 с разным содержанием кроссагента. [35] |
Малая избирательность сорбции четвертичных аммониевых оснований сульфосефадексами имеет аналогию и в сорбции большей части других ионов органических веществ на ионообменных сефадексах и биогелях. [36]
Для высокоэффективной ГПХ низкомолекулярных веществ, а также олигомеров обычно используют набухающие сшитые гели: декстрановые гели - сефадексы, полиакриламидные гели - биогели Р для ГПХ в воде или водных растворах, поливинилаце-татные гели ( меркогели) и стирогели ( порогели) для неводных гидрофобных систем. Оксипропилированный сефадекс LH-20 может быть использован как в водных, так и в неводных растворах. [38]
В таком же количестве раствора размешивают 8 г сефадекса G-75, 4 г сефадекса G-100, 4 г биогеля Р60 и 3 5 г биогеля РЗОО. Чтобы гель набух, его выдерживают 2 - 3 сут при 4 С, после чего непродолжительное время вакуумируют, используя водоструйный насос. С помощью устройства для нанесения сорбента фирмы Desaga ( системы Шталя) наносят слои толщиной 0 5 мм; если жидкой фазы было взято больше, как в данном случае, то поверхность слоя остается гладкой. Слои сушат на воздухе 5 - 15 мин и помещают в камеру с увлажненной атмосферой, где их можно хранить до 2 недель. Непосредственно перед употреблением пластинки обрабатывают соответствующим буферным раствором, лучше всего в течение ночи. [39]
Наиболее широкое распространение среди носителей для гель-хроматографии белков получили сорбенты, приготовленные на основе декстрана ( сефадексы, сефакрилы, молселекты), полиакриламида ( биогели Р, акрилексы) и агарозы ( сефарозы, биогели А) и др. Набухая в воде, они образуют гели. [40]
Гель-проникающую хроматографию компонентов нуклеиновых кислот проводят на сшитых декстрановых гелях ( сефадек-сах) ( Sephadex, Pharmacia, Uppsala, Sweden) и полиакриламид-ных гелях ( биогелях) ( Bio-Gel, Bio-Rad Labs Richmond, Calif. Кроме того, гели обладают ионообменными и адсорбционными свойствами, проявляя повышенное сродство к ароматическим и гетероциклическим соединениям. [41]
Жесткие гели типа биогеля Р-2, которые практически не меняют своих свойств при значительном повышении давления, можно использовать в качестве сорбентов при ВЭЖХ, тогда как более мягкие гели, например биогель Р-300, теряют в этих; условиях механическую прочность. Большое число работ, выполненных в последнее время, посвящено исследованию возможности применения для фракционирования полисахаридов более жестких сорбентов, не изменяющих своих характеристик при: высоких давлениях. Наиболее перспективным в этом направлении является, по всей видимости, использование таких неорганических сорбентов как стекло или силикагель, каждый из которых можно получить в виде гранул строго определенного-размера. [42]
Ситовая ( гель-фильтрационная) хроматография связана в основном с различием в скоростях диффузии молекул и макромолекул компонентов смеси в поры соответствующих сорбентов, в частности набухающих органических пористых полимеров - сефадексов, биогелей, а также ненабухающих макропористых си-ликагелей или силохромов и макропористых стекол. В этом случае вещества с большими молекулярными весами, образующие наиболее крупные частицы, практически не диффундируют в поры и поэтому злюируют первыми. Удерживаемые объемы таких веществ на подходящих по размерам пор ситах увеличиваются с уменьшением их молекулярных весов или объемов. [43]
Наиболее широкое распространение среди носителей для гель-хроматографии белков получили сорбенты, приготовленные на основе декстрана ( сефадексы, сефакрилы, молселекты), полиакриламида ( биогели Р, акрилексы) и агарозы ( сефарозы, биогели А) и др. Набухая в воде, они образуют гели. [44]
Ограниченная деформируемость поверхностей каналов и пустот создает условия для возникновения полифункционального взаимодействия, в результате чего подобные иониты не только способны поглощать большое количество макромолекул различных белков, но и в отличие от ионообменных сефадексов и биогелей избирательно сорбируют белки и ферменты. Сорбционная емкость этих ионитов по отношению к белкам падает весьма незначительно при увеличении концентрации буферных электролитов в растворе. [45]
Страницы: 1 2 3 4