Интенсивно желтая окраска
Cтраница 1
Интенсивно желтая окраска образующейся натриевой соли re - нитрофенола свидетельствует о наличии этих соединений. Для повышения чувствительности реакции можно воспользоваться реагентом Миллона, который с фенолами и фенолкарбоновыми кислотами дает малиново-красное окрашивание. [1]
Интенсивно желтую окраску аниона этого соединения в бикарбо-натном растворе ( А Макс 440 нм) используют для его обнаружения и фотометрического определения. Для проведения определения экстракт, полученный извлечением вещества из растений или продуктов петролейным эфиром, подвергают обработке 0 1 % - ным раствором NaHCO3 и затем колориметрируют. [2]
Метод основан на образовании интенсивно желтой окраски при взаимодействии нитрофенолов - ( NO2) C6H4OH со щелочью. [3]
Во время титрования при переходе интенсивно желтой окраски в бледно-желтую в колбу прибавляют несколько капель раствора крахмала. Раствор окрашивается в синий цвет и титруется до обесцвечивания. [4]
Аналитически перекись водорода легко обнаруживается по интенсивно желтой окраске, которую она сообщает раствору сульфата титана. [5]
Аналитически перекись водорода легко обнаруживается по интенсивно желтой окраске; которую она сообщает раствору сульфата титана. [6]
Например, очень прочное соединение Fe2 - ферроцен имеет интенсивно желтую окраску, диамагнитно, нейтрально, легко плавится, перегоняется без разложения, нерастворимо в воде и способно вступать в самые разнообразные реакции замещения без разрушения молекулы. Таким образом, оно обладает ярковыра-женным ароматическим характером. [7]
Перекись титана даже в ничтожных концентрациях сообщает водному раствору интенсивно желтую окраску. Ее образованием ( в сильнокислой среде) пользуются поэтому как чрезвычайно чувствительной реакцией и на титан и на перекись водорода. Ответственным за окраску является, по-видимому, ион TiOj, содержащий пероксидную группу в трехчленном цикле с титаном. Содержащий кристаллизационную перекись водорода ТЮ ( С1О4Ь НгОа бесцветен. [8]
Перекись титана даже в ничтожных концентрациях сообщает водному раствору интенсивно желтую окраску. Ее образованием ( в сйльнркислой среде) пользуются поэтому как чрезвычайно чувствительной реакцией и на титан и на перекись водорода. Содержащий кристаллизационную перекись водорода ТЮ ( С1О4) 2 - Н2О2 бесцветен. [9]
Желтые красители трудно титровать, так как тартрат титана имеет интенсивно желтую окраску. [10]
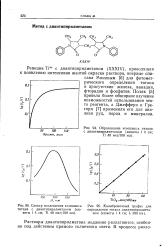 |
Образование комплекса титана.| Спектр поглощения комплекса [ IMAGE ] Калибровочный график для. [11] |
Реакция Ti4 с диантипирилметаном ( XXXIV), приводящая к появлению интенсивно желтой окраски раствора, впервые описана Мининым [6] для фотометрического определения титана в присутствии железа, ванадия, фторидов и фосфатов. [12]
Факел, полученный с ламинарным потоком газа, имел цилиндрическую - форму, интенсивно желтую окраску и напоминал цветом и формой диффузионный факел цилиндрической горелки. [13]
В слабокислых растворах перманганат вызывает исчезающую темнозеленую окраску, в сильнокислых растворах появляется устойчивая интенсивно желтая окраска продукта окисления бензидина. На 5 мл титруемого раствора добавляют 1 каплю ( 0 03 мл) раствора бензидина. [14]
Тетрахлорид титана Т1СЦ представляет собой бесцветную или слабоокрашенную в желтый цвет жидкость, дымящуюся на воздухе, растворимую в воде л во многих органических жидкостях - бензоле, толуоле, хлороформе и др. Под действием видимого и УФ-света цвет TiCU может принимать более интенсивно желтую окраску. [15]
Страницы: 1 2 3