Оксалат - плутоний
Cтраница 1
Оксалат плутония Pu2 ( C2O4) 3 выпадает в виде гидрата Ри2 ( С2О4) з - 9Н2О при действии оксалата натрия на растворы солей трехвалентного плутония. Полное осаждение плутония при концентрации оксалата в маточном растворе 0 2 М достигается через 30 мин. Растворимость оксалата сильно возрастает с увеличением кислотности раствора. [1]
 |
Константы нестойкости оксалатных комплексов плутония ( IV. [2] |
Собственно оксалат плутония ( IV) плохо растворим в воде ( 20 мг / л раствора), но постепенно растворяется в избытке осадителя. [3]
Растворение оксалата плутония ( IV) в избыточном количестве карбоната калия, натрия или аммония приводит к образованию темно-зеленых растворов комплексных плутонийкарбонатов. [4]
Гексагидрат оксалата плутония ( IV) плохо растворяется в минеральных кислотах и очень хорошо в растворах оксала-тов и карбонатов щелочных металлов и аммония с образованием комплексных соединений. [5]
Процесс термического разложения оксалата плутония ( IV), изучавшийся рядом авторов [32], характеризуется следующими превращениями. [6]
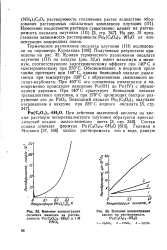 |
Влияние концентрации.| Влияние концентрации. [7] |
Кривая термического разложения оксалата плутония ( III) на воздухе ( рис. 32 а) имеет максимум и минимум, соответствующие эндотермическому эффекту при 140 С и экзотермическому при 270 С. Обезвоживание в инертной среде также протекает при 140 С, однако безводный оксалат разлагается при температуре 330 С с образованием смешанного ок-салат-карбоната. При 460 С это соединение разлагается и одновременно происходит окисление Pu ( III) до Pu ( IV) с образованием двуокиси. Безводный оксалат Ри2 ( С2О4) з получают нагреванием в вакууме при 225 С водного оксалата [ 3, стр. [8]
Тот факт, что оксалат плутония ( III) растворим в избытке щавелевокислого калия или аммония, указывает на комплексообразование в этой среде. [9]
При нагревании на воздухе оксалат плутония в интервале температур от 30 до 110 С теряет 6 молекул воды. [10]
Если в такой темно-зеленый раствор продолжать вводить оксалат плутония, то последний, растворяясь, постепенно изменяет окраску раствора: она становится зеленовато-коричневой, красно-бурой н, наконец, красной, после чего оксалат плутония перестает растворяться. Смешанные комплексные соединения были нами выделены и подвергнуты исследованию. [11]
Изменение кислотности раствора существенно влияет на растворимость оксалата плутония ( III) [ 3, стр. На рис. 31 представлена зависимость растворимости Ри2 ( С2О4) з 9Н2О от концентрации водородных ионов. [12]
Трибромид плутония РиВгз получается аналогично РиС13 или нагреванием оксалата плутония ( III) ( высушенного при 50 С) в токе бромистого водорода при 600 С. [13]
Для выяснения вопроса о влиянии количества добавляемого карбоната на состав смешанных комплексов плутония навеска оксалата плутония растворялась полностью в 10 % - ном растворе соды, а затем добавлялся це значительный избыток содового 10 % - ного раствора, не изменяющий заметно красно-бурого цвета раствора. Таким образом было получено подтверждение того, что количество растворителя не влияет на общее число анионов во внутренней сфере получающегося комплекса. [14]
В этой системе обогащение твердой фазы микрокомпонентом ( D 22) происходит при значительно меньшей растворимости оксалата плутония ( - 90 раз) по сравнению с оксала-том лантана. [15]
Страницы: 1 2 3