Оксалат - плутоний
Cтраница 2
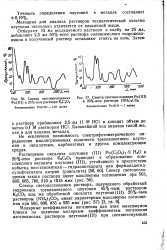 |
Спектр светопоглощения Pu ( III в 20 % - номрастворе К2С2О.| Спектр светопоглощения Ри ( III в 20 % - ном растворе ( NHihCOa. [16] |
Спектр светопоглощения раствора, полученного обработкой гидроокиси трехвалентного плутония 45 % - ным раствором КаСО3 или же обработкой оксалата плутония ( III) 20 % - ным раствором ( МЬЦЬСОз, имеет характерные максимумы поглощения при 565, 600, 835 и 920 ммк ( рис. 57) [ 3, гл. [17]
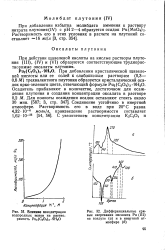 |
Влияние концентрации водородных ионов на растворимость Pu2 ( C2O4 з.| Дифференциальные кривые нагревания оксалата Ри ( III на воздухе ( а и в инертной атмосфере ( б. [18] |
При действии щавелевой кислоты на кислые растворы плутония ( III), ( IV) и ( VI) образуются соответствующие труднорастворимые оксалаты плутония. [19]
Если в такой темно-зеленый раствор продолжать вводить оксалат плутония, то последний, растворяясь, постепенно изменяет окраску раствора: она становится зеленовато-коричневой, красно-бурой н, наконец, красной, после чего оксалат плутония перестает растворяться. Смешанные комплексные соединения были нами выделены и подвергнуты исследованию. [20]
Двуокись плутония Ри02 имеет цвет от желто-зеленогосдо коричневого и является стабильным окислом плутония. Оксалат плутония ( III) превращается в двуокись только при температуре выше 800 С. [21]
Четырехвалентный плутоний количественно осаждается в виде шестиводного оксалата [ 48, стр. Растворимость оксалата плутония ( IV) существенно понижается в присутствии этилового спирта. Метод позволяет определять плутоний в присутствии большинства элементов за исключением тория, циркония и редкоземельных элементов. [22]
Наименее загрязненную двуокись плутония с составом, почти отвечающим стехиометрии, получают при прокаливании пе-роксида плутония и оксалатов трех - и четырехвалентного плутония [ 3, стр. Прокаливание высушенных кристаллических оксалатов плутония ( III) и ( IV) и пероксида плутония ( IV) производят при медленном повышении температуры от 25 до 700 С. Для предотвращения распыления осадка вследствие идущих одновременно процессов обезвоживания и разложения пероксид плутония ( IV) необходимо нагревать в интервале температур от 90 - 200 С особенно осторожно. Сульфат-ион, входящий в структуру пероксида плутония ( IV), улетучивается в виде 5Оз при 600 - 700 С. Оксалаты плутония следует прокаливать при температуре не ниже 900 - 950 С. Как уже отмечалось, для получения двуокиси плутония стехиометрического состава во всех случаях прокаливание проводят при 1050 - 1200 С. [23]
Особенно сильно сказывается саморадиолиз на физико-химических свойствах соединений таких интенсивных излучателей, какими являются заурановые элементы. Так, оксалат плутония за полтора года хранения практически полностью превращается в оксикарбонат. Оксалат же америция полностью превращается в карбонат всего за 20 суток. Радиоактивный ( по Agno) азид серебра с удельной активностью 3 5 мкюри / г детонирует в полтора раза быстрее, чем нерадиоактивный препарат. [24]
Особенно сильно сказывается саморадиолиз на физико-химических свойствах соединений таких интенсивных излучателей, какими являются заурановые элементы. Так, оксалат плутония за полтора года хранения практически полностью превращается в оксикарбонат. Оксалат же америция полностью превращается в карбонат всего за 20 суток. Радиоактивный ( по Ag110) азид серебра с удельной активностью 3 5 мкюри / г детонирует в полтора раза быстрее, чем нерадиоактивный препарат. [25]
Исходные карбонатные растворы Ри ( IV) легко получались растворением какой-либо соли Ри ( IV) в водном растворе карбоната калия, натрия или аммония. Большая растворимость оксалата плутония в карбонатном растворе и резкое изменение окраски раствора позволяли легко следить за комплексообразованием и получать весьма концентрированные растворы комплексных соединений. [26]
При действии на двуокись плутония хлорирующих реагентов ( CCU, РС, SC12) при высокой температуре ( 500 - 700 С) образуется сравнительно летучий трихло-рид плутония, возгоняющийся из зоны реакции. Он образуется при действии газообразного хлористого водорода на оксалат плутония ( III) или его гидрид при 400 С. При выпаривании растворов Puds с последующим нагреванием в токе хлористого водорода получается безводная соль. [27]
Дело в том что растворимость оксалата калия, образующегося в результате реакции оксалата плутония с поташом, достаточно велика, а сравнительно невысокая концентрация последнего способствует тому, что весь образовавшийся оксалат калия находится в растворе. Такие растворы окрашены в красно-бурый цвет, что указывает на присутствие смешанного карбонатно-оксалатного комплексного соединения. [28]
Таким образом, были подтверждены выводы о влиянии общей концентрации анионов СОз2 и С2С42 - в растворе на состав образующегося комплексного соединения плутония. Следует отметить, что методика замены карбонат-ионов на оксалат-ионы действием твердой щавелевой кислоты, по-видимому, может быть применена для получения таких соединений, как, например, К12 [ Ри ( С204) 8 ] - Н20, которые обычным путем - путем растворения оксалата плутония в оксалате калия - до сих пор не получены. [29]
Из раствора ( после отделения урана) осаждают плутоний, например щавелевой кислотой. Незначительные отклонения от этих условий приводят к существенным потерям плутония вследствие увеличения его растворимости. Этот метод представляет интерес, так как благодаря растворимости оксалата плутония в кислой среде можно проводить ряд последовательных осаждений. При каждом осаждении содержание у-активных элементов уменьшается примерно в 20 раз. [30]
Страницы: 1 2 3