Оксалат - церие
Cтраница 3
В случае невыпадения осадка раствор необходимо нагреть. После добавления соли тория под действием щавелевой кислоты обязательно должен выпасть осадок оксалата тория, вместе с которым будет соосаждаться и оксалат церия. [31]
Оксалат тория не растворяется в разбавленных кислотах и очень медленно, лучше при нагревании, растворяется в концентрированных. Оксалат цирконила также не растворяется в разбавленных кислотах, но растворяется в концентрированных. Оксалат церия в присутствии из ытка иона С2О4 не растворяется в разбавленных кислотах на холоду. В концентрированных кислотах оксалат церия растворяется. [32]
При определенном избытке щавелевой кислоты коэффициент А сохраняет постоянное значение, не зависящее от количества осажденного носителя. С увеличением концентрации щавелевой кислоты А заметно возрастает. Хотя растворимость оксалата церия в тех условиях, которые соответствуют табл. 1, значительно выше растворимости оксалата урана, наблюдается обогащение твердой фазы церием. [33]
Соединения железа ( III), алюминия, хрома и урана препятствуют осаждению церия и, вероятно, других редкоземельных металлов в виде их оксалатов, если не прибавить очень большого избытка осадителя. Соли указанных металлов растворяют оксалат церия, но избыток щавелевой кислоты или оксалата аммония осаждает его снова. В приводимом здесь методе анализа это мешающее влияние железа ( III), алюминия, хрома и урана не может проявиться. [34]
Из солянокислого раствора аммиаком, не содержащим С02, осаждаются гидроокиси Fe, Al, Ce, Y, La, редкоземельных элементов, диуранат и диплутонат аммония. Осадок гидроокисей, полученный переосаждением едким натром, не содержащий алюминия, растворяется в соляной кислоте. После разбавления водой до концентрации НС1 0 3 г-экв / л производится осаждение оксалатов церия, иттрия и редкоземельных элементов. Церий, после перевода в четырехвалентное состояние, отделяется от иттрия в виде иодата. [35]
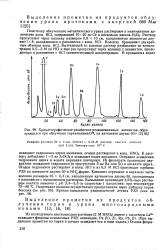 |
Хроматографическое разделение редкоземельных элементов, образующихся при облучении тория ионами О16, на катионите дауэкс - 50Х 12. [36] |
К раствору добавляют 1 - 2 мг ZrOCla и осаждают иодат циркония. Операции осаждения гидроокиси церия и иодата циркония повторяют. Из фильтрата производят двукратное осаждение гидроокиси ( в присутствии 5 мг Ва или Sr) и оксалата церия. Осадок гидроокиси растворяют в конц. [37]
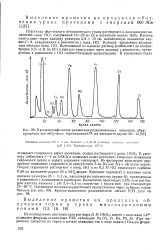 |
Хроматографическое разделение редкоземельных элементов, образующихся при облучении тория ионами О16, на катионите дауэкс - 50Х 12 [ 16J. [38] |
К раствору добавляют 1 - 2 мг ZrOCb и осаждают иодат циркония. Операции осаждения гидроокиси церия и иодата циркония повторяют. Из фильтрата производят двукратное осаждение гидроокиси ( в присутствии 5 мг Ва или Sr) и оксалата церия. Осадок гидроокиси растворяют в конц. [39]
Остатки гидрохинона устраняют добавлением Н202 в аммиачном растворе и последующей обработкой конц НС. Добавлением оксалатов выделяют церий, не загрязненный органическими остатками. Оксалат церия затем растворяют в конц. [40]
Растворимость оксалатов церия, тория и цирконила в минеральных кислотах различна. Оксалат тория не растворяется в разбавленных кислотах и очень медленно, лучше при нагревании, растворяется в концентрированных. Оксалат цирконила также не растворяется в разбавленных кислотах, но растворяется в концентрированных. Оксалат церия в присутствии избытка иона С2О4 не растворяется в разбавленных кислотах на холоду. В концентрированных кислотах оксалат церия растворяется. [41]
Оксалат тория не растворяется в разбавленных кислотах и очень медленно, лучше при нагревании, растворяется в концентрированных. Оксалат цирконила также не растворяется в разбавленных кислотах, но растворяется в концентрированных. Оксалат церия в присутствии из ытка иона С2О4 не растворяется в разбавленных кислотах на холоду. В концентрированных кислотах оксалат церия растворяется. [42]
Метод основан на нерастворимости иодата четырехвалентного церия в азотной кислоте определенной концентрации. К холодному раствору нитрата редкоземельных элементов приливают конц. Церий осаждается в виде желтого хлопьевидного осадка иодата четырехвалентного церия. Раствор кипятят со щавелевой кислотой до прекращения выделения паров пода; при этом осаждается оксалат церия. Осадок оксалата оставляют стоять на ночь. Недостатком метода является то, что процесс осаждения иодата церия приходится повторять несколько раз для отделения соседних редкоземельных элементов, особенно празеодима. [43]
Метод основан на нерастворимости иодата четырехвалентного церия в азотной кислоте определенной концентрации. К холодному раствору нитрата редкоземельных элементов приливают конц. Церий осаждается в виде желтого хлопьевидного осадка иодата четырехвалентного церия. Раствор кипятят со щавелевой кислотой до прекращения выделения паров пода; при этом осаждается оксалат церия. Осадок оксалата оставляют стоять на ночь. Недостатком метода является то, что процесс осаждения подата церия приходится повторять несколько раз для отделения соседних редкоземельных элементов, особенно празеодима. [44]
Часто используемым методом выделения радиоактивных изотопов из растворов является соосаждение их с труднорастворимыми осадками. К недостаткам методов осаждения относится их невысокая избирательность: часто с труднорастворимым осадком соосаждаются изотопы различных элементов. Для очистки изотопа, полученного посредством осаждения, от изотопов-примесей приходится добавлять в раствор носители элементов-примесей и прибегать к переосаждению осадка, часто неоднократному. Примером использования методов осаждения может служить выделение изотопов редкоземельных элементов соосаждением с фторидом или оксалатом церия. [45]
Страницы: 1 2 3 4