Оксалоацетат
Cтраница 2
 |
Малат-аспартатнаячелночная система для переноса восстанавливающих эквивалентов от цитозольного НАДН в митохондриальный матрикс. Объяснение в тексте. [16] |
Транспортирование в цитозоле регенерирует Оксалоацетат, что вызывает к действию следующий цикл. В целом процесс включает легкообратимые реакции, происходит без потребления энергии, движущей силой его является постоянное восстановление НАД в цитозоле гли-церальдегид-3 - фосфатом, образующимся при катаболизме глюкозы. [17]
Ацетил - КоА превращается в оксалоацетат через глиоксилатный цикл ( гл. [18]
Использование глюкозы и ее предшественника оксалоацетата для образования молока в условиях активного катаболизма жирных кислот приводит к кетозу. Жвачные могут легко превращать про-пионат в сукцинил - СоА ( рис. 20 - 7) и далее в оксалоацетат, что предотвращает кетоз. [19]
Сукци-натдегидрогеназа способна связывать в активном центре оксалоацетат с чрезвычайно высоким сродством. Процесс диссоциации ингибитора очень медленный, особенно при низких температурах. В свази с этим при измерении любых активностей митохондриальных ферментов, в которых участвует дегидрирование сукцината, необходимо быть уверенным, что сукцинатдегидрогеназа находится в активном состоянии. Пре-инкубацию проводят при - 30 С в течение 30 мин. За это время происходит полное вытеснение оксалоацетата из активного центра фермента. Этот процесс называют активацией сукцинатдегидрогеназы. [20]
В цитозоле в этой реакции возникает оксалоацетат, который не имеет транспортных систем возврата внутрь митохондрии, так как мембрана для этого соединения непроницаема. В цитозоле есть фермент - малатдегидрогеназа, восстанавливающая оксалоацетат до малата, который по дикарбоксилат-транспортной системе возвращается в митохондриальный матрикс. [21]
В связи с тем что для оксалоацетата мембрана митохондрии непроницаема, уже в цитоплазме он восстанавливается посредством НАДН в малат, который при участии специфической транслоказы может вернуться в матрикс митохондрии, где окисляется до оксалатацетата. Таким образом, завершается так называемый челночный механизм транспорта ацетила через метохондриальную мембрану. Восстановленный НАДФН наряду с ацетил - КоА и С02 используется в синтезе жирных кислот. [22]
Этот синтез, ведущий от пирувата через Оксалоацетат к фосфоенол-пирувату, требует двух высокоэнергетических фосфатов: одного для карбоксилирования пирувата, а другого-для образования фосфоенолпирувата из оксалоацетата. [23]
Однако в присутствии повсеместно распространенной НАД-специфичной малатдегидрогеназы оксалоацетат и малат легко превращаются друг в друга. Реакция, катализируемая ФЕП-кар-боксикиназой, легко обратима, тогда как реакция, катализируемая ФЕП-карбоксилазой, фактически необратима; отсюда следует, что ФЕП-карбоксилаза в сочетании с малатдегидрогена-зой, по-видимому, может обеспечить клетки высокоэффективным ферментативным механизмом для синтеза малата. ФЕП-карбоксилаза была впервые выявлена в ряде тканей растений, не относящихся к семейству толстянковых, однако она особенно активна в листьях Kalanchoe, Bryophyllum и Sedum. Интересно, что до сих пор нет данных, которые бы доказывали, что она присутствует в животных клетках. ФЕП-карбоксикиназная активность обнаружена в экстрактах из многих растений, однако в листьях Kalanchoe и Bryophyllum она пока не найдена. [24]
Радиоактивный СО2 включается сначала в Отсоединения - оксалоацетат, малат и ас-партат. Максимальная скорость включения СО2 у этих растений может достигать 40 - 60 мг СО2 на квадратный дециметр поверхности листа в час ( - 0 3 ммоль СО2 на м 2 - 1, или - 0 10 моль СО2 на 1 моль суммарного хлорофилла в 1 с), что вдвое выше, чем для большей части сельскохозяйственных растений. [25]
 |
Схема путей, ведущих от изолей-цина, метионина и валина к сукцинил - СоА. [26] |
Остающийся углеродный скелет аспартата, в форме оксалоацетата, включается в цикл лимонной кислоты. [27]
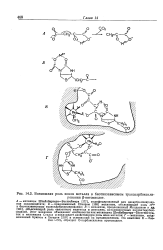 |
Возможная роль ионов металла в биотинзависимом транскарбоксили. [28] |
А-механизм Штейнбергера-Вестгеймера [177], модифицированный для декарбоксилирова-ния оксалоацетата; Б - предложенный Стилсом [198] механизм, объясняющий роль МЧ-в биотинзависимом транскарбоксилировании; В - механизм, предложенный Милдваном и др. [201], объясняющий роль связанного марганца в реакциях, катализируемых пируваткарбок-силазой. Этот механизм объединяет особенности как механизма Штейнбергера-Вестгеймера, так и механизма Стилса и показывает двойственную роль иона металла; Г - механизм, предложенный Брюсом и Хегарти [210] и основанный на предположении, что комплекс Е - био тин - СО2 образует О-карбоксильное производное. [29]
Страницы: 1 2 3 4
