Оксид - тип
Cтраница 2
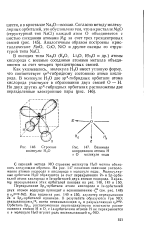 |
Взаимная координация атомов Н и О молекуле воды. [16] |
В оксидах типа Na2O ( K2O, Li2O, Rb2O и др.) атомы кислорода с восемью соседними атомами металла объединяются за счет четырех трехцентровых связей. [17]
В оксидах типа Na2O ( K2O, Rb O, Li2O) атомы кислорода ( за счет 2s, 2pv -, 2ру - и 2р2 - орбиталей) с восемью соседними атомами металла объединяются посредством четырех трехцентровых связей. [18]
 |
Перекрывание атомных орбиталей в оксидах со структурой типа NaCl. [19] |
В оксидах типа Na2O ( КаО, Rb2O, Li2O) атомы кислорода ( за счет 2s, 2рж -, 2pv - и 2рг - орбиталей) с восемью соседними атомами металла объединяются посредством четырех трехцентровых связей. [20]
Из них оксиды типа Э2О5 и соответствующие им гидроксиды имеют кислотные свойства, ослабляющиеся от мышьяка к висмуту, и окислительные свойства, которые усиливаются от мышьяка к висмуту. [21]
Они образуют оксиды типа Э2О3 и гид-роксиды Э ( ОН) 3, которые проявляют амфотерные свойства. Основные свойства оксидов и гидроксидов в подгруппе усиливаются сверху вниз, а кислотные свойства - ослабляются. [22]
Все лантаниды образуют оксиды типа - твердые, кристаллические, тугоплавкие вещества, характеризующиеся высокими энтальпиями образования. [23]
Все лантаниды образуют оксиды типа Э2Оз - твердые, кристаллические, тугоплавкие вещества, характеризующиеся высокими энтальпиями образования. [24]
В кристаллической решетке оксидов типа Mi - xO ( NiO, Cu2O, CoO, FeO) дефицит металла связан с избыточными ионами кислорода в междоузлиях О или вакансиями в ка-тионной подрешетке VM. Наличие последних определяет дырочную проводимость этих оксидов, являющихся полупроводниками р-типа. Максимальное отклонение от стехиометрии возникает на границе оксида с электролитом. [25]
Все элементы VA-группы имеют оксиды типа Э2О5 и гидроксиды НЭО3 или НзЭО4, которые обладают кислотными свойствами. Кроме того, для них характерны оксиды типа Э2О3 и соответствующие гидроксиды НЭО2 или Н3ЭО3; у азота и фосфора они имеют кислотные свойства, у мышьяка и сурьмы амфотерны, а у висмута проявляют основной характер. [26]
Все элементы VA-подгруппы имеют оксиды типа Э2О5 и гидроксиды НЭО3 или Н3ЭО4, которые обладают кислотными свойствами. Кроме того, для них характерны оксиды типов Э2О3 и соответствующие гидроксиды НЭО2 или Н3ЭО3; у азота и фосфора они имеют кислотные свойства, у мышьяка и сурьмы амфотерны, а у висмута проявляют основной характер. [27]
Мышьяк и сурьма образуют оксиды типа Э2О5 только при действии сильных окислителей. При гидролизе 5ЬС15 получается коллоидный раствор сурьмяной кислоты. [28]
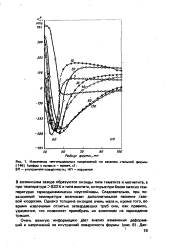 |
Изменение тангенциальных напряжений по сечению стальной формы. [29] |
В возникшем зазоре образуются оксиды типа гематита и магнетита, а при температуре 833 К и типа вюстита, которые при более низких температурах термодинамически неустойчивы. Следовательно, при повышенной температуре возникает дополнительное явление газовой коррозии. Однако толщина оксидов очень мала и, кроме того, во время извлечения отлитых затвердевших труб они, как правило, удаляются, что позволяет пренебречь их влиянием на зарождение трещин. [30]
Страницы: 1 2 3 4