Органические оксикислота
Cтраница 3
Известно, что пятивалентная сурьма совсем н е растворима либо очень мало растворяется в пищевых и органических кислотах. Трехвалентная сурьма легко растворяется при действии органических оксикислот, образуя комплексные соединения типа рвотного камня. [31]
Ализарин красный S в кислом растворе образует осадок красно-фиолетового цвета; при малом количестве циркония появляется красно-фиолетовое окрашивание. Реакции, кроме того, мешают фториды, сульфаты, фосфаты, органические оксикислоты, а также молибдаты и вольфраматы. [32]
Большинство других элементов вообще не дают осадков с ферроцианидом или образуют белые осадки, не мешающие открытию урана. Маскирующие уран комплексообразователи: фторид, карбонат, ацетат, цитрат и анионы других органических оксикислот обесцвечивают окраску. [33]
В последние годы получены новые стимуляторы роста: гибберел-лины ( открыты в выделениях грибка gibberella fujikuroi), обладающие высокой физиологической активностью в крайне незначительных концентрациях ( 1 - 100 вес. Обнаружены гиббе-реллины А ], Аг, Аз, А4 и др; они представляют сложные органические оксикислоты. [34]
Комплекс циркония с ализариновым красным С ( ализарин-сульфонат натрия) в кислых растворах имеет красно-коричневый цвет в присутствии избытка ализаринового красного С и фиолетовый цвет в присутствии избытка циркония. Комплекс обесцвечивается в присутствии фторида, фосфата, арсената, сульфата, тиосульфата, оксалата и других органических оксикислот. Чувствительность метода ниже чувствительности двух первых описанных выше методов, однако простота выполнения анализа этим методом делает его пригодным для целей рутинного анализа. Так как примеси в воде влияют на результаты анализа, требуется предварительная обработка анализируемых проб. [35]
Взаимодействие циркония с реактивом арсеназо I, предложенным В. И. Кузнецовым, рассмотрено на стр. При рН 1 5 - 1 8 мешает титан, а также F -, SOf, органические оксикислоты, ослабляющие или уничтожающие окраску. [36]
Интенсивность окраски в присутствии 1000 мкг / мл А1 или Sn соответствует 0 075 или соответственно 0 3 мкг / мл Zr. Фосфаты, фториды и органические оксикислоты мешают определению. [37]
В последние гуды получены новые стимуляторы роста гиббе-реллнпы ( открыты в выделениях грибка gibberella fujikuroi. Обнаружены гиб-береллины AI, А. А; они предстасляют сложные органические оксикислоты. [38]
Ализарин красный S в кислом растворе образует осадок красно-фиолетового цвета; при малом количестве циркония появляется красно-фиолетовое окрашивание. Бериллий, алюминий, титан и торий также дают красно-фиолетовую окраску, следовательно, мешают открытию циркония. Реакции, кроме того, мешают фториды, сульфаты, фосфаты, органические оксикислоты, а также молибдаты и вольфраматы. [39]
Техника изготовления и свойства силикагелей зависят от того, что хотя кремнекислый ион в водных растворах щелочных силикатов сильно гидратирован и выделяется действием сильных кислот, образуемый при этом гидрат кремневой кислоты чрезвычайно неустойчив. Хотя он имеет склонность к дегидратации даже в присутствии избытка воды в разбавленных растворах, но в нейтральных растворах при нормальной температуре скорость дегидратации очень мала. Далее надо отметить, что ( как это имеет место в отношении многих слабых органических оксикислот) дегидратация проходит предпочтительно между прилежащими молекулами, а не внутри одной и той же молекулы. [40]
Преимущество арсеназо перед другими реагентами типа R - ОН состоит в том, что в его состав входит остаток мышьяковой кислоты, поэтому арсеназо способен взаимодействовать с Zr в более кислой среде, чем ализарин S, так как образование арсенатов циркония легко происходит уже в сильнокислых растворах. Кроме того, остаток мышьяковой кислоты способствует ускорению реакции. При добавлении водного раствора арсеназо к растворам Zr в 0 08 - 0 1 N НС1 розовая окраска переходит в фиолетовую. Кроме Zr и Ш при этих же значениях рН дает цветную реакцию и титан. Мешают реакции F, SO42 и органические оксикислоты, ослабляющие окраску. Измерения производятся на ФЭК с желтым светофильтром с областью пропускания 550 - 572 ммк. [41]
К капле исследуемого ( по возможности близкого к нейтральному) раствора в микротигле прибавляют каплю раствора реагента и нагревают до кипения. В присутствии циркония появляется красная или фиолетовая окраска. Такую же окраску могут дать алюминий, бериллий, титан и торий. Если прибавить каплю разбавленной соляной кислоты, то остается только окрашенное соединение циркония красно-фиолетового или красно-бурого цвета. Кроме фторидов, обнаружению циркония мешают сульфаты, фосфаты и органические оксикислоты. [42]
Наносят по 1 капле испытуемого раствора, как описано выше, на две пластинки. После развития окраски на одну из пластинок со смесью растворов вносят кристаллы фторида натрия и перемешивают. При этом исчезает окраска комплекса циркония с пи-рокатехиновым фиолетовым. Изменение окраски указывает на присутствие циркония. Большинство катионов маскируется прибавлением комплексона III. Мешают Sb ( III) и Sn ( V), которые в присутствии комплексона III могут быть отделены аммиаком, а также большие количества урана и органические оксикислоты. Мешающее действие фтор-ионов может быть элиминировано бериллием. [43]
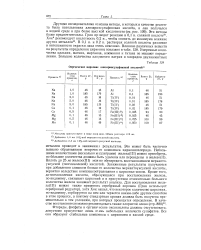 |
Определение цирконш ализаринсульфоновой кислотой 8. [44] |
Это может быть частично вызвано образованием непрочнсго комплекса цирконилхлорида. Вплоть до 25 мг железо ( Ш) можно обезвредить восстановлением меркаптоуксусной ( тиогликолевой) кислотой. Заниженные результаты получаются при добавлении слишком большего количества меркаптоуксусной кислоты, вероятно вследствие комплексооСразования с цирконил-ионом. Кроме того, дитиогликолевая кислота, образующаяся при восстановлении железа, по-видимому, связывает цирконий и в присутствии относительно большого количества железа занижает результат анализа. Для восстановления желе-за ( Ш) можно также применять серебряный порошок ( Грин использует серебряный редуктор), хотя Хок нашел, что некоторое количество циркония, по-видимому, сорбируется на нем или теряется каким-либо другим способом в этом процессе, а поэтому стандартная кривая должна быть получена применительно к тем условиям, при которых проводится определение. В качестве восстановителя можно рекомендовать также хлористое олово ( стр. Фториды, фосфаты и органические оксикислоты должны отсутствовать; допустимо присутствие лишь очень небольших количеств сульфатов. Все они образуют стабильные комплексы с цирконием в кислой среде. [45]
Страницы: 1 2 3 4