Оксихлорид - цирконий
Cтраница 1
Оксихлорид циркония кристаллизуется в виде соединения ZrOCl2 - 8H20, хорошо растворимого в воде, но слабо растворимого в соляной кислоте. [1]
Оксихлорид циркония - соединение, из которого легко можно получить другие соединения циркония. Например, прокаливанием его на воздухе получают двуокись циркония. Технологический процесс кристаллизации оксихлорида прост. [2]
Безводные оксихлориды циркония и гафния получить довольно трудно. [3]
Навеску оксихлорида циркония 0 88 г растворяют в 40 мл соляной кислоты, разбавляют в мерной колбе вместимостью 250 мл водой до метки и перемешивают. Аликвотную часть раствора ( 50 мл) помещают в стакан вместимостью 250 мл, разбавляют водой до 100 мл, добавляют к раствору 1 г хлорида аммония, нагревают смесь до 70 С и приливают по каплям раствор аммиака при перемешивании до появления запаха. Раствор с осадком нагревают до кипения, дают постоять 20 мин в теплом месте, затем отфильтровывают на фильтре с белой лентой. [4]
Растворимость оксихлорида циркония сильно зависит от концентрации соляной кислоты и температуры. Затем раствор охлаждают, и 95 % циркония кристаллизуется. [5]
Катализатором служил оксихлорид циркония, нанесенный на силикагель. [6]
При взаимодействии оксихлорида циркония ( гафния) в водном растворе с низшими карбоновыми кислотами ( муравьиной, уксусной, пропионовой) образуются двузамещенные соединения типа MeO ( CH3COO) 2 - 3H2O, хорошо растворяющиеся в воде, но не растворяющиеся в органических растворителях. Циркониевые и гафниевые мыла в воде не растворяются, не гидролизуются, как правило, полимеризованы. [7]
При взаимодействии оксихлорида циркония ( гафния) в водном растворе с низшими карбоновыми кислотами ( муравьиной, уксусной, пропионовой) образуются двузамещенные соединения типа МеО ( СНзСОО) 2 ЗН2О, хорошо растворяющиеся в воде, но не растворяющиеся в органических растворителях. Циркониевые и гафниевые мыла в воде не растворяются, не гидролизуются, как правило, полимеризованы. [8]
Катализатором: служил оксихлорид циркония, нанесенный на снликагель. [9]
Известны также и другие оксихлориды циркония. [10]
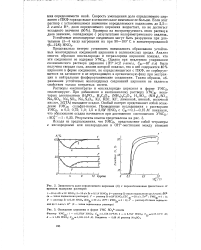 |
Зависимость доли определяемого циркония ( А с пирокатехиновым фиолетовым от времени выдержки растворов.| Осаждение циркония в форме УМС 5О42 - - ионом. [11] |
Растворы оксинитрата и оксихлорида циркония в форме УМСгг опалесцируют. [12]
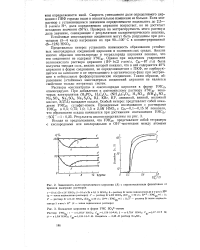 |
Зависимость доли определяемого циркония ( Л с пирокатехиновым фиолетовым от времени выдержки растворов.| Осаждение циркония в форме УМС 5О42 - ионом. [13] |
Растворы оксинитрата и оксихлорида циркония в форме УМС2г опалесцируют. При добавлении к азбтнокислому раствору УМС2г некоторых электролитов ( Н3РО4, Н2С2О4, ( NH4) 2C2O4, H2SO4, ( NH4) 2SO4, Na2SO4, Na2SO3, Na2S2O3, KJ, KBr, KF, лимонной, винной, молочной кислот, ЭДТА) выпадают осадки. Особый интерес представляет собой осаждение УМС2г сульфат-ионом. [14]
Экстракция проводилась из растворов оксихлорида циркония ( гафния) в 2 5 - 5 0-мол. [15]
Страницы: 1 2 3 4