Оксогалогениды
Cтраница 3
Помимо чисто галоидных соединений, для ванадия и ниобия характерны оксогалогениды общей формулы ЭОГз. [31]
В большинстве случаев эти соединения малоустойчивы, часто взрывчаты; более устойчивы оксогалогениды, диоксогало-гениды А. [32]
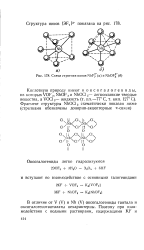 |
Схема строения ионов NbF ( а и NbOF ( б. [33] |
В отличие от V ( V) и Mb ( V) оксогалогениды тантала и оксогалогенотанталаты нехарактерны. [34]
Известны простые да - и тетра-галогениды 8пХ2 и 8пХ4 ( см. табл.), смешанные галогениды 8пХ Х - , оксогалогениды, а также комплексные-галогене-станнаты. [35]
Названия галогенангидридов образуются по-разному, в зависимости от того, рассматривать ли данное соединение как гало-генангидрид, или как галогенид ( или оксогалогенид) соответствующего элемента. Так, соединение РОС13 может быть названо либо трихлорангидридом ортофосфорной кислоты, либо-трихлороксидом фосфора ( V); точно так же соединение РВг3 можно назвать трибромангидридом фосфористой кислоты, бромидом фосфора ( III) или трехбромистым фосфором. [36]
Рутений и осмий значительно легче, чем железо, переходят в высшие состояния окисления ( VI и VIII); в химии этих элементов очень важное место занимают четырехокиси АЮ4 ( а также оксогалогениды и оксо-анионы. [37]
Из них MoFj образуется при восстановлении MoFs молибденом при нагревании, МоСЬ получается при восстановлении МоСЬ с помощью Hj или Mo; МоВгз и Mob образуются при взаимодействии молибдена соответственно с бромом и иодом. Известны также оксогалогениды МоОГ 4Н20 ( F-F, CI, Вг) и гексагалогеномолибдаты мЛМоГб ] ( Г - F, О. [38]
Оксогалогениды того или иного типа известны Для большинства металлов периодической системы, за исключением щелочных и, возможно, металлов Ш - подгруппы. В табл. 10.10 приведены известные оксогалогениды металлов групп VA-VIIA и VIII; это преимущественно соединения с фтором и хлором, очень редко - с иодом. В ходе дальнейшего развития химии такое положение может, разумеется, измениться. [39]
 |
Кристаллографические формы двуокиси кремния, устойчивые при давлении 1 атм. [40] |
Кроме этих линейных оксо-галогенидов, известны также циклические оксогалогениды, такие, как ( SiOX2) 4, в которых имеются восьмичленные кольца чередующихся атомов кремния и кислорода. [41]
 |
Кристаллографические формы двуокиси кремния, устойчивые при давлении 1 атм. [42] |
Кроме этих линейных оксо-галогенидов, известны также циклические оксогалогениды, такие, как ( SiOX) 4, в которых имеются восьмичленные кольца чередующихся атомов кремния и кислорода. [43]
 |
Структура фрагмента [ MsXi2 ] n, свойственная многим галогенидным соединениям низковалентных ниобия и тантала. [44] |
Тетрахлориды являются кислотами Льюиса. Тетрахлорид тантала TaCU легко отрывает кислород и дает оксогалогениды, но - NbCl4 может реагировать с оксо-лигандами, образуя при этом. [45]
Страницы: 1 2 3 4