Оксокарбонат
Cтраница 2
 |
Зависимость молярного соотношения концентрации карбонат-ионов и висмута в осадке от значения я в системе при обработке оксокарбоната висмута растворами гидроксида. [16] |
Исследования по взаимодействию оксокарбоната висмута с растворами щелочных реагентов показали, что при обработке оксокарбоната водными растворами аммиака состав его не меняется. На кривой зависимости А - п при А 0 33 имеется пологий участок, отвечающий образованию оксогидроксокарбоната висмута. [17]
Хорошо изучены простые M ( CN), и комплексные [ M ( CN) J2 - цианиды, а также карбонаты и оксокарбонаты. [18]
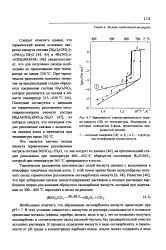 |
Зависимость электропроводности оксида висмута ( III от температуры. Измерения, в которых появляется р-фаза, представлены прерывистой линией. [19] |
В этих условиях совместно с висмутом из раствора соосаждаются и основные примесные металлы ( свинец, серебро, железо, медь и др.), что не позволяет получать оксокарбонат и соответственно оксид высокой чистоты без предварительной очистки исходных растворов. [20]
Эндоэффект при 730 С обусловлен полиморфным превращением a - BiaOs в высокотемпературную модификацию 8 - В1гОз, а эндоэффект при 824 С соответствует плавлению оксида. Согласно данным [168], разложение оксокарбоната на воздухе протекает в интервале 400 - 530 С. [21]
Проведенное нами сравнение способов получения оксида висмута из оксогидроксонитрата состава [ В1бС5 ( ОН) з ] ( МОз) 5 - ЗН2О, полученного в результате осаждения висмута из азотнокислых растворов в области рН 1 0 - - 2 0, при его обработке как растворами гидро-ксида натрия, так и другими щелочными реагентами ( аммиаком или карбонатом аммония) показало [65], что обработка оксогидроксонитрата висмута раствором гидро-ксида натрия при 85 5 С в течение 2 ч при весовом отношении Ж: Т равном 4: 1 ( расход NaOH 1 50 % от стехиометрии) позволяет перевести его в оксид. Однако получаемый продукт частично содержит висмут в виде оксокарбоната, для перевода которого в оксид необходимо прокаливание продукта при 420 40 С. В результате обработки оксогидроксонитрата висмута растворами аммиака с концентрацией 2 моль / л ( 250 % от стехиометрии) при 85 5 С в течение 2 ч образуются оксогид-роксонитрат состава [ В1бО7 ( ОН) 2 ] ( МОз) 2 - 2Н2О, в котором соотношение Bi к нитрат-ионам равно 3: 1, и для перевода в оксид необходимо его прокаливание при температуре не ниже 520 С. Повторная обработка оксогидроксонитрата растворами аммиака позволяет перевести его в оксид, но продукт, как и в случае обработки растворами гидроксида натрия, содержит в виде примеси оксокарбонат висмута. [22]
Основными преимуществами метода щелочной дегидратации азотнокислых солей висмута по сравнению с используемым в промышленности методом термического разложения при 690 30 С являются устранение выделения в атмосферу токсичных оксидов азота и существенное снижение энергозатрат. Однако при этом необходима многократная промывка продукта водой для очистки от ионов щелочных металлов, а также не исключена возможность загрязнения оксида оксокарбонатом висмута. [23]
Однако при разложении оксогидроксонитрата висмута имеет место плотная упаковка малых зерен, имеющих размер в диаметре от 2 до 10 мкм, в то время как при разложении оксокарбоната возникает рыхлая, с большим количеством пор, упаковка оплавленных микрозерен размером 1 мкм и меньше. [25]
Считается, что ( 3 - Bi2O3 не может быть получена при комнатной температуре. Однако в ряде работ отмечено, что р-фазу можно получить при обычной температуре: при добавлении растворов солей висмута в щелочные растворы [17], а также при термическом разложении оксокарбоната, субсалицилата или галлата висмута. Так, например, по данным Левина и Рота [6], разложение оксокарбоната состава В12О2СОз при 400 С в течение 18 ч приводит к образованию тетрагональной модификации оксида висмута, которую в данном случае можно сохранить до комнатной температуры. При термическом разложении субсалицилата и субгаллата висмута при температуре ниже 400 С имеет место образование тетрагональной модификации оксида висмута, стабильной до комнатной температуры. В [19] приведены данные по синтезу метастабильного при обычных условиях 3 - В12Оз различными способами низкотемпературной обработки: разложением ВЮ2 при 320 - 380 С; прокаливанием оксокарбоната состава ( ВЮ) 2СОз; окислением на воздухе мелкораздробленного металлического висмута при 370 - 400 С; быстрым добавлением раствора нитрата висмута в кипящий раствор гидроксида натрия, взятого в избытке. [26]
Оксокарбонат висмута может быть синтезирован непосредственным осаждением Bi при рН 8 добавлением висмутсодержащих азотнокислых или солянокислых растворов к растворам карбонатов натрия или аммония. Однако совместно с висмутом осаждаются и основные примесные металлы ( свинец, серебро, железо, цинк и др.), что не позволяет получать продукт высокой чистоты. Вследствие этого для получения оксокарбоната высокой чистоты в качестве исходного сырья требуется использовать предварительно очищенный металлический висмут или его оксид. [27]
Считается, что ( 3 - Bi2O3 не может быть получена при комнатной температуре. Однако в ряде работ отмечено, что р-фазу можно получить при обычной температуре: при добавлении растворов солей висмута в щелочные растворы [17], а также при термическом разложении оксокарбоната, субсалицилата или галлата висмута. Так, например, по данным Левина и Рота [6], разложение оксокарбоната состава В12О2СОз при 400 С в течение 18 ч приводит к образованию тетрагональной модификации оксида висмута, которую в данном случае можно сохранить до комнатной температуры. При термическом разложении субсалицилата и субгаллата висмута при температуре ниже 400 С имеет место образование тетрагональной модификации оксида висмута, стабильной до комнатной температуры. В [19] приведены данные по синтезу метастабильного при обычных условиях 3 - В12Оз различными способами низкотемпературной обработки: разложением ВЮ2 при 320 - 380 С; прокаливанием оксокарбоната состава ( ВЮ) 2СОз; окислением на воздухе мелкораздробленного металлического висмута при 370 - 400 С; быстрым добавлением раствора нитрата висмута в кипящий раствор гидроксида натрия, взятого в избытке. [28]
 |
Проекция поликатиона [ В 2О ( ОН2 ] наосьа. [29] |
Из диаграммы состояния системы Na2SO4 - В12 ( 8О4) з следует, что соединение NaBi ( SO4) 2 плавится инконгруэнтно при 680 С, а эвтектика Na2SO4 - NaBi ( SO4) 2 плавится при 640 С. В [124] кислый сульфат висмута состава HBi ( SO4) 2 - 3H2O был синтезирован в результате растворения оксокарбоната висмута в избытке горячей 60 % - й серной кислоты ( d 1 505 г / см) с последующим выдерживанием выпавших игольчатых кристаллов в маточном растворе в течение суток, их отфильтровыванием и промывкой этиловым спиртом. [30]
Страницы: 1 2 3
