Искаженный октаэдр
Cтраница 1
 |
Наиболее обычные структуры ионов металлов в их комплексах. [1] |
Искаженный октаэдр с четырьмя короткими и двумя длинными ( более слабыми) связями или реже с двумя короткими и четырьмя длинными связями. В пределе структура становится плоской квадратной. [2]
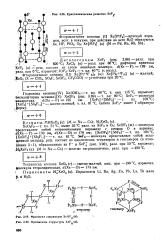 |
Кристаллическая решетка XeF.| Фрагмент структуры XeOF ( к. [ IMAGE ] фрагменты структуры XeF ( к. [3] |
XeF-молекула представляет собой искаженный октаэдр, реш. С, взрывчат; ( к) ( М Na - Cs) - желтые гигроскопичные, разл. [4]
Среди несколько искаженных октаэдров распределены ионы Na, которые занимают два положения: одна треть из них - Na ( l) имеет шестикратную координацию по отношению к ионам фтора при расстоянии Na ( l) - F - 0 221 нм и находится на середине ребер элементарной ячейки. Две трети других ионов - Na ( 2) находятся внутри элементарной ячейки и окружены 12 ионами F - при расстоянии Na ( 2) - F - 0 268 нм. [5]
 |
Структура трирути-ла ( структурный мотив V2 [ WOe ] и CrJWOe ]. [6] |
Но образуют они не искаженный октаэдр, а правильную триго-нальную призму с расстояниями W-О 1 95 А, что практически совпадает со средним значением аналогичных расстояний в вольфрам-кислородных октаэдрах. Переход от октаэдрической к тригонально-призматической координации приводит, естественно, к некоторому укорочению расстояний О... О в комплексе [ W0e ] e -; в данном случае они равны 2 45 и 2 58 А. [7]
Си находятся в центре искаженных октаэдров. Аналогичные соединения, содержащие ионы металлов, которые не обнаруживают эффекта Яна - Теллера ( например, Ni11 или Zn), имеют кубическую структуру, в которой атомы металлов окружены правильными октаэдрами. Интересно отметить, что в двух соединениях с хлором, приведенных в таблице, четыре короткие связи имеют одинаковую длину, в то время как длинные связи сильно отличаются от них. На примере других соединений также видно, что короткие связи имеют постоянную длину, соответствующую как бы радиусу иона Си в этих направлениях, а длинные либо ненамного, либо существенно превышают длину коротких связей. Теоретически это можно ожидать, поскольку степень искажения зависит от многих факторов, действующих в каждом отдельном соединении. Так, можно полагать, что квадратная координация, обнаруженная в СиО и многих комплексах Си, является предельным случаем октаэдра, искаженного в результате эффекта Яна - Теллера, а не новым типом координации. [8]
Ионы Си2 находятся внутри ромбически искаженного октаэдра. Октаэдры связаны между собой короткими сторонами экваториальных прямоугольников в цепи, расположенных вдоль оси а. [9]
Каждый ион Си окружен искаженным октаэдром, состоящим из четырех молекул Н20 и двух О с тетрагональной симметрией. Две оси тетрагональной системы расположены примерно под прямыми углами одна к другой, поэтому кристалл в магнитном смысле не является аксиальным. [10]
Если шесть лигандов в искаженном октаэдре неодинаковые, то возникает вопрос: какие из них будут расположены на нормальных расстояниях от иона металла и какие будут более уда-лепными в ( 4 2) - координации. [11]
Ва соответствующие атомы О образуют сильно искаженный октаэдр. [12]
Атом Со находится в центре искаженного октаэдра, образованного атомом С1, группой NH3, двумя атомами азота групп NO2 и двумя атомами азота бидентатной группы этилендиамина. Расстояния внутри комплекса в основном согласуются с литературными данными. Молекула этилендиамина имеет гош-строение. [13]
Его молекула имеет форму несколько искаженного октаэдра. [14]
Анион этого перксената имеет структуру слегка искаженного октаэдра со средним расстоянием d ( XeO) 1 85 А. Тетранатрийперксенат может быть выделен в виде бесцветного кристаллогидрата с 6 или 8 Н20, который обезвоживается около 100 С, а бурно разлагается лишь при 360 С. Соль эта малорастворима в воде ( растворимость около 0 025 / И), но сильно гидролизуется, давая щелочную реакцию. [15]
Страницы: 1 2 3 4 5