Искаженный октаэдр
Cтраница 3
Атом рутения находится в окружении шести лигандов, образующих сильно искаженный октаэдр. [31]
Анализ квадрупольных расщеплений в низкоспиновых комплексах железа с симметрией искаженного октаэдра можно провести, если детально известна соответствующая схема образования связей. [32]
Катионы Mg2 окружены шестью концевыми атомами 0 -, образующими искаженный октаэдр, а катионы Са2 - четырьмя концевыми и четырьмя мости-ковыми атомами О. [33]
С / - могли бы рассматриваться как частные случаи конфигурации искаженный октаэдр; поскольку, однако, они допускают значительные изменения валентных углов, их целесообразно считать самостоятельными формами координационных сфер. [34]
В рутиле атомы титана октаэдрически окружены атомами кислорода; несколько искаженные октаэдры [ ТЮ61, имеющие по два общих ребра, образуют цепи, параллельные оси с. В анатазе октаэдры искажены более сильно, имеют по четыре общих ребра и образуют спиральные цепи вдоль осей. Различная устойчивость модификаций двуокиси титана может быть объяснена на основании третьего правила Полинга: Наличие в структуре у координационных полиэдров общих ребер и особенно общих граней уменьшает устойчивость структуры. Уменьшение стабильности структуры связано с уменьшением расстояния между атомами титана, находящимися в центрах октаэдров, усилением отталкивания между ними и деформацией октаэдров. [35]
В рутиле атомы титана октаэдрически окружены атомами кислорода; несколько искаженные октаэдры [ TiO6 ], имеющие по два общих ребра, образуют цепи, параллельные оси с. В анатазе октаэдры искажены более сильно, имеют пэ четыре общих ребра и образуют спиральные цепи вдоль осей. Различная устойчивость модификаций двуокиси титана может быть объяснена на основании третьего правила Полинга: Наличие в структуре у координационных полиэдров общих ребер и особенно общих граней уменьшает устойчивость структуры. Уменьшение стабильности структуры связано с уменьшением расстояния между атомами титана, находящимися в центрах октаэдров, усилением отталкивания между ними и деформацией октаэдров. [36]
Основная структурная единица кристалла состоит из иона Fe3 в окружении искаженного октаэдра, образованного из двух ионов и четырех молекул воды. Реальный кристалл составляют два типа таких октаэдров. Соответственно существуют два направления градиентов электрического поля в элементарной ячейке кристалла. [37]
В структуре корунда все ионы А13 лежат вдоль тригональной оси искаженного октаэдра, образованного шестью ионами кислорода. Тригональное искажение расщепляет основное состояние 3Tig иона V3 ( рис. 11 - 6, б) на орбитально синглетное состояние Azg, занимающее низший уровень, и орбитально дважды вырожденное состояние Е8, расположенное на 1200 см 1 выше. Сильное спин-орбитальное взаимодействие с этим низколежащим возбужденным состоянием приводит к короткому времени TI, поэтому необходимо проводить измерения ЭПР при 4 К и ниже. [38]
 |
Диаграммы энергетических уровней, демонстрирующие возможные высокоспиновые и низкоспиновые основные состояния для системы d ( например, Ni2 в тетрагонально искаженном октаэдрическом поле. [39] |
На рис. 26.11 6 показано возможное расположение уровней в сильно тетрагонально искаженном октаэдре или в предельном случае такого искажения - в квадратном четырехкоординационном комплексе ( ср. Вследствие большой разницы в энергии высшей занятой и следующей за ней свободной cf - орби-тали у реальных ионоз d8, например у Ni, Pd, Pt, Rh1, Ir1 и Аи1, высокоспиновая конфигурация невозможна. [40]
 |
Длины связей ( А в структурах МО ( ОН. [41] |
Таким образом, каждый атом железа имеет координационный многогранник в виде искаженного октаэдра, образованный атомами кислорода, и эти октаэдры объединены с образованием гофрированных слоев. Атомы водорода в этой структуре не были локализованы, однако на основании известного окружения атомов кислорода можно идентифицировать О - и ОН-группы. [42]
Катионы Си2 окружены тремя ОН-группами и тремя ионами СР, образуя также искаженный октаэдр, причем три гид-роксила и один ион СР лежат в плоскости искаженного квадрата, а остальные два иона СР находятся на значительно большем расстоянии. [43]
Каждый атом кобальта в этом соединении находится в окружении групп, образующих искаженный октаэдр, причем ацетиленовая углерод-углеродная связь почти перпендикулярна связи кобальт-кобальт, а оба атома кобальта и оба атома углерода ацетиленовой группы расположены почти тетраэдрически. [44]
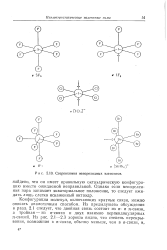 |
Стереохимия непереходных элементов. [45] |
Страницы: 1 2 3 4 5