Искаженный октаэдр
Cтраница 4
Однако если неподеленная пара занимает экваториальное положение, то следует ожидать лишь слегка искаженный октаэдр. [46]
 |
Схема отроения Cr04 ( NH3 3.| Квадратная антипризма.| Строение иона [ Мо ( СМ8 ] 4 -. [47] |
По-видимому, единственным исключением является молекула ХеГе, для которого вероятна структура искаженного октаэдра. [48]
По-видимому, единственным исключением является молекула XeFe, для которого вероятна структура искаженного октаэдра. С другой стороны, они же характерны для ионов [ SeCle ] 2 и [ ТеСЦ ] 2, в которых каждый из центральных атомов имеет свободную электронную пару. [49]
По его данным, она сходна со структурой МоО2 и состоит из искаженных октаэдров VO6, которые, попарно сочленяясь ребрами, образуют цепи. Расстояния между атомами ванадия в цепях неодинаковы и составляют 2 65 или 3 12 А. [50]
 |
Характеристики F-структур и ансамблей I-структур кластеров Na ( H2O n и К ( Н20 п. [51] |
В кластерах с КЧ 6 молекулы воды расположены вокруг ионов по вершинам слегка искаженных октаэдров. Между молекулами воды, образующими первую гидратнуго оболочку иона Na в / - - структурах, водородная связь никогда не образуется. Среди / - структур кластеров К ( Н2О) иногда возможны такие, в которых молекулы первой гидратной оболочки соединены водородной связью. Молекулы воды, принадлежащие ко второй гидратной оболочке, образуют, естественно, водородные связи как друг с другом, так и с молекулами, составляющими ближайшее окружение иона. [52]
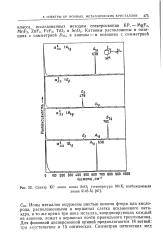 |
Спектр КР окиси олова SnO2 ( температура 100 К, возбуждающая. [53] |
Ионы металлов окружены шестью ионами фтора или кислорода, расположенными в вершинах слегка искаженного октаэдра, в то же время три иона металла, координирующих каждый из анионов, лежат в вершинах почти правильного треугольника. [54]
 |
Характеристики F-структур и ансамблей 1-структур кластеров Na ( H O n и К ( Н2О п. [55] |
В кластерах с КЧ 6 молекулы воды расположены вокруг ионов по вершинам слегка искаженных октаэдров. Между молекулами воды, образующими первую гидратную оболочку иона Na в F-структур ах, водородная связь никогда не образуется. Среди F-структур кластеров K ( H2O) иногда возможны такие, в которых молекулы первой гидратной оболочки соединены водородной связью. Молекулы воды, принадлежащие ко второй гидратной оболочке, образуют, естественно, водородные связи как друг с другом, так и с молекулами, составляющими ближайшее окружение иона. [56]
Каждый атом Sn в этой структуре окружен шестью другими атомами Sn по искаженному октаэдру с четырьмя ближайшими соседями на расстоянии 3 016 А и двумя другими на расстоянии 3 175 А. [57]
Ко второй группе относятся уранаты, атомы кислорода в которых расположены по вершинам искаженного октаэдра, ураниловая связь направлена вдоль его оси четвертого порядка. Если два октаэдра имеют один общий атом кислорода, не входящий в ураниловую группировку, то образуются тетрагональные или псевдотетрагональные уранил-кислородные сетки ( см. рис. 3.1, а), между которыми находятся атомы металла. В случае соединения октаэдров ребрами образуется уранил-кис-лородный мотив, включающий бесконечные цепочки. [58]
Предполагается строение сольвата в виде VO ( НаО), имеющего симметрию сильно тетрагонально искаженного октаэдра, поскольку связь V - О является очень прочной и, видимо, гораздо более короткой, чем другие. [59]
Предполагается строение сольвата в виде VO ( Н2О), имеющего симметрию сильно тетрагонально искаженного октаэдра, поскольку связь V - О является очень прочной и, видимо, гораздо более короткой, чем другие. [60]
Страницы: 1 2 3 4 5