Электронный октет
Cтраница 2
 |
Строение кристалла алмаза.| Слоистая решетка графита. [16] |
Оно отражает стремление атомов элементов к образованию электронного октета. Свинец представляет исключение из этого правила; он кристаллизуется в решетке кубической плотной упаковки. [17]
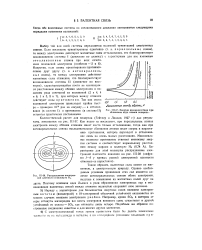 |
Энергия взаимодействия при сближении двух атомов водорода.| Распределение электрон ной плотности в молекуле Н2. [18] |
Наряду с характерным для большинства инертных газов внешним электронным октетом ( восьмеркой) и 18-электронной оболочкой устойчивой оказывается во многих случаях внешняя электронная двойка. Например, кроме 5Оз, в котором от серы оттянуты кислородом все шесть электронов внешнего слоя, существует и другой устойчивый ее окисел - SO2) где оттянуты лишь четыре. Подобным же образом построенные соединения известны и для многих других элементов. [19]
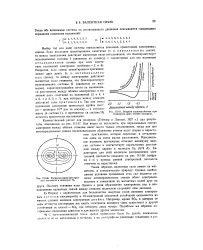 |
Энергия взаимодействия при сближении двух атомов водорода.| Распределение электронной плотности в молекуле Н2. [20] |
Наряду с характерным для большинства инертных газов внешним электронным октетом ( восьмеркой) и 18-электронной оболочкой устойчивой оказывается во многих случаях внешняя электронная двойка. Например, кроме SOs, в котором от серы оттянуты кислородом все шесть электронов внешнего слоя, существует и другой устойчивый ее окисел - SOa, где оттянуты лишь четыре. Подобным же образом построенные соединения известны и для многих других элементов. [21]
Наряду с характерным для большинства инертных газов внешним электронным октетом ( восьмеркой) и 18-электронн ой оболочкой устойчивой оказывается во многих случаях внешняя электронная двойка. [22]
Известен ряд других устойчивых ионных комплексов, в которых электронный октет атома кремния расширен за счет образования дополнительных связей Si - О. Центральный атом кремния в них связан лишь с электроотрицательными атомами либо, в крайнем случае, с одним, органическим радикалом. [23]
Каждый атом ( внутри пунктирного контура) характеризуется укомплектованным электронным октетом. При этом четвертая электронная пара, осуществляющая ковалентную связь, поставляется атомами Bv за счет неподеленных 2-электронов. [24]
По теории Льюиса - Лэнгмюра ( 1916 - 1918) электронные октеты ( дублет у водорода) образовывались общими парами электронов, принадлежавшими обоим атомам. [25]
Когда углерод образует 8 - А / - СВЯЗИ, электронный октет вокруг атома состоит из четырех пар поделенных электронов. У азота, образующего три связи, существует одна неподеленная пара. Однако, когда бор образует три ковалентные связи, группа валентных электронов состоит из трех поделенных пар. Природа этих связей неизвестна, но, вероятно, в них использованы орбиты sup, поскольку они симметрично распределены в плоскости. Соединения бора такого типа легко присоединяют нейтральные молекулы, например NH, и CH3CN, образуя ( CHS) 3B - NH3 и BC13 - NC - CH8, где атомы бора имеют поэтому четыре связи. Радиус бора, вычисленный из расстояний В - С в В ( СН3) 8, равен 0 79 А. [26]
Таким образом, инертность этих элементов, обусловленная необычайной устойчивостью электронного октета, и нулевая валентность их ( кроме гелия и неона) оказались иллюзорными. Так как для этих газов известны соединения с валентностью 8, они должны быть включены в VIIIA-группу периодической системы на правах полноправных элементов, обретших свою химическую индивидуальность. [27]
Наличие у атома серы неподеленной пары электронов и возможность расширения электронного октета за счет участия d - орбит обусловливают двойственный характер поведения атома серы в реакциях сульфидов. [28]
Согласно схеме, четыре сг-электрона и четыре я-электрона являются связевыми, составляя электронный октет, принадлежащий молекуле в целом. В антисвязевой области лежат лишь шесть электронов: одна 0-пара и две я-пары. Непарных электронов в молекуле F2 не имеется. [29]
В теории Льюиса - Лэнгмюра ( 1916 - 1918) стремление к электронному октету ( дублету у водорода) удовлетворялось образованием общей пары ( или нескольких пар) электронов, принадлежавшей обоим атомам. [30]
Страницы: 1 2 3 4