Октилфенол
Cтраница 3
Зависимость изменения кислотного числа и выделения сероводорода сохраняется при взаимодействии октилфенола с пятисернистым фосфором, в интервале температур 60 - 140 С. [31]
Растворяют 2 1 г ( 0 01 М) n - октилфенола в 140 мл этилового спирта. [32]
Их выделяют спиртом из расплавов диметилоль-ных производных тг-тгереот-бутилфенола и n - октилфенола, образующихся при 130 - 140 С. При фракционированном разделении спирторастворимых циклических продуктов поликонденсации из смеси продуктов с преимущественным содержанием ге-пгретге-бутил-диоксиметилфенола было выделено соединение с температурой плавления 245 С. [33]
Это предположение подтверждено измерениями55 давления пара растворов ( 9 7) оксиэтилированного октилфенола. [34]
Алкилфенолы с большой алкильной группой, как, например, бутилфенол, амилфенол октилфенол, дают смолы, растворимые в масле. [35]
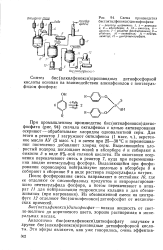 |
Схема производства бис ( октилфенокси дитиофосфата. [36] |
При промышленном производстве бис ( октилфенокси) дитиофосфата ( рис. 94) сначала октилфенол с целью активирования осерняют - обрабатывают хлоридом одновалентной серы. С и перемешивании постепенно добавляют хлорид серы. Выделяющийся хлористый водород поглощают водой в абсорбере 4 и собирают в емкости 5 в виде 8 % - ной соляной кислоты. По окончании осернения перекачивают смесь в реактор 7, куда при перемешивании вводят пентасульфид фосфора. Выделяющийся при фосфи-ровании сероводород нейтрализуют щелочью в абсорбере 8 и собирают в сборнике 9 в виде раствора гидросульфида натрия. [37]
Промышленное алкилирование фенола тримером пропилена или диизобутиленом для получения соответственно нонил - и октилфенола проводят в присутствии трехфтористого бора. К фенолу добавляют около 0 5 - 2 % BF3 и начинают подавать алкен с такой скоростью, чтобы максимальная температура реакции не превышала 4О - 45 С для октилфенола и 55 - 60 С для нонилфенола. Более высокие температуры облегчают образование диалкилированных фенолов и других побочных продуктов. После завершения реакции катализатор разлагают, отмывая его водой и затем раствором соды. Полученную смесь перегоняют, чтобы выделить целевой продукт и отделить его от избытка фенола. [38]
Промышленное алкилирование фенола тримером пропилена или диизобутиленом для получения соответственно нонил - и октилфенола проводят в присутствии трехфтористого бора. К фенолу добавляют около 0 5 - 2 % BF3 и начинают подавать алкен с такой скоростью, чтобы максимальная температура реакции не превышала 40 - 45 С для октилфенола и 55 - 60 С для нонилфенола. Более высокие температуры облегчают образование диалкилированных фенолов и других побочных продуктов. После завершения реакции катализатор разлагают, отмывая его водой и затем раствором соды. Полученную смесь перегоняют, чтобы выделить целевой продукт и отделить его от избытка фенола. [39]
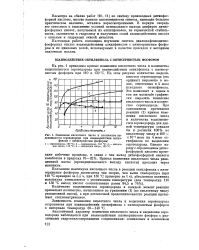 |
Изменение кислотного числа и количества выделившегося сероводорода при взаимодействии октилфенола с пятисернистым фосфором. [40] |
На рис. 1 приведены кривые изменения кислотного числа и количества выделившегося сероводорода при взаимодействии октилфенола с пятисернистым фосфором при 110 и 130 С. [41]
На рис. 1 приведены кривые изменения кислотного числа и количества выделившегося сероводорода при взаимодействии октилфенола с пятисернистым фосфором при 110 и 130 С. На этом рисунке количество выделившегося сероводорода ( ось ординат) выражено в молях, отнесенных к 4 моль исходного октилфенола. Это позволяет в одном и том же масштабе графически выразить изменение кислотного числа и количество сероводорода. [42]
Октилфенолы применяются в качестве азосоставляющих для получения оранжевых дисазокрасителей для шерсти и шелка по схеме: октилфенол - бензидиндисульфокислота - нафтолсульфокислота. [43]
Так, например, гексилфенол обладает максимальной активностью по отношению к тифозным бактериям, а гептил-и октилфенолы лучше действуют на бактерии Staphylococcus aureus, гексилфенол действует на них менее активно. [44]
Композиция, состоящая из 69 % мыльных стружек, 25 % оксиэтилированного n - mpem - октилфенола и 6 % n - mpem - октилфе-нолгликолевого эфира. [45]
Страницы: 1 2 3 4