Биосинтез - аминокислота
Cтраница 3
Подобные явления репрессии и ретроингибирования действуют на многих путях биосинтеза аминокислот. [31]
 |
Аллостерические белки имеют два различных центра связывания. Если один из них занят, то по второму связывание не происходит. [32] |
Все, что мы только что узнали о регуляции биосинтеза аминокислот, без существенных поправок верно и для биосинтезов других веществ. Но синтез - это только одна сторона обмена веществ, связанная с потреблением строительных материалов и энергии. Другая сторона обмена - это процессы, поставляющие энергию в результате расщепления, разложения пищи; при этом клетка получает основные строительные материалы и энергию. Зададимся вопросом, не регулируются ли процессы распада точно так же, как процессы синтеза, и притом посредством аналогичных регуляторных систем. [33]
Более пятидесяти лет назад Кнооп постулировал, что при биосинтезе аминокислот имеет место восстановительное аминирование кетокислот. [34]
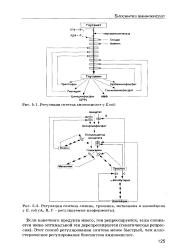 |
Регуляция синтеза аминокислот у E. coli.| Регуляция синтеза лизина, треонина, метионина и изолеицина у.. coii ( А, В, С - регулируемые изоферменты. [35] |
Этот способ регулирования синтеза менее быстрый, чем алло-стерическое регулирование биосинтеза аминокислот. [36]
Прямое аминирование кетокислот аммиаком - первая и наиболее важная реакция биосинтеза аминокислот. Позднее в ряде исследований В. Л. Кре-товича была показана возможность такого биосинтеза аминокислот у многих растений, и был выделен ферментный препарат, катализирующий синтез аланина из аммиака и пировиноград-ной кислоты. [37]
В этом разделе мы рассмотрим их использование при изучении механизма биосинтеза аминокислот с разветвленными боковыми цепями - валина и изолейцина. [38]
Полученную в результате разделения биомассу, содержащую белки, ценные для биосинтеза аминокислот и ростовые факторы, целесообразно возвращать в качестве компонента питательной среды либо для глубинного культивирования различных продуцентов ферментов, либо для твердофазного культивирования микроскопических грибов - продуцентов ферментов. Такая операция позволяет заменить в составе пиательной среды дефицитные компоненты, например, кукурузный экстракт или дрожжи, значительным образом улучшить состав воздушного бассейна, снизить нагрузку на очистные сооружения. [39]
Распад липидов, как и распад углеводов, обеспечивает исходные соединения для биосинтеза аминокислот ( а из них белков) и поддерживает образование белков энергетически. [40]
Известно, что у сальмонелл, например, структурные гены для 10 ферментов биосинтеза аминокислоты гистидина сцеплены в одном опероне. Подобное сцепление функционально связанных генов, как мы уже знаем, характерно для бактерий. [41]
Пировииоградпая к-та играет важную роль в процессе обмена веществ, при распаде и биосинтезе аминокислот белка; образуется в тканях животного организма при окислительном распаде углеводов и жиров, в процессе дезаминирова-ния аминокислот. Пировиноградпая к-та под влиянием ферментов присоединяет С02 с образованием щаве-левоуксусной к-ты, участвующей в цикле трикарбо-новых к-т, играющем важную роль при окислении углеводов. [42]
Переаминирование ( А. Е. Браунштейн, М. Г. Крицман, 1937 г.) играет ведущую роль в процессе биосинтеза аминокислот в растениях: аммиак, образующийся при восстановлении нитритов и нитратов или в результате жизнедеятельности микроорганизмов, ами-нирует при участии ферментов кетоглутаровую кислоту, которая превращается в глутаминовую кислоту, являющуюся донором аминогрупп при синтезе других аминокислот. [43]
Некоторые промежуточные продукты цикла, в частности а-кетоглутарат, сукцинат и оксалоацетат могут использоваться как предшественники в биосинтезе аминокислот. Многие из этих реакций обратимы, так что они служат одновременно и для образования промежуточных продуктов цикла из аминокислот. [44]
У жвачных животных значит, часть мочевины поступает из крови в рубец, где она используется микрофлорой для биосинтеза аминокислот, к-рые поступают в кровь животного. Без участия микроорганизмов эти животные не способны утилизировать своб. Такой процесс избавляет верблюда от потерь воды, неизбежных при выделении мочевины с мочой. [45]
Страницы: 1 2 3 4